Fuego y calor, esas materias inexistentes
La naturaleza última de dos fenómenos físicos omnipresentes, el fuego y el calor, desconcertó a los filósofos naturales hasta mediados del siglo XIX. La pregunta de si el agente del calor, que podía funcionar sin emitir luz, era diferente de la causa del fuego, al que los antiguos habían dado estatus de elemento fundamental de todo lo existente, se convirtió en insistente a finales del XVIII.
Cuando los protoquímicos del XVII eliminaron el fuego de la lista de principios simples que constituían toda la materia, retuvieron la idea de que el fuego era el agente más eficaz del que disponían para alterar o reducir la materia. No era para menos, los procedimientos sofisticados de destilación les permitían aplicar el fuego con un control muy fino.
Si bien unos pocos químicos y filósofos naturales, incluyendo a Francis Bacon, consideraban el fuego y el calor como expresiones del movimiento de las partículas de la materia ordinaria, la mayoría creía que eran una sustancia, o sustancias, especial. En la filosofía newtoniana se pensaba que esta sustancia estaba compuesta por partículas que se repelían entre sí pero que eran atraídas por la materia ordinaria. Por ello se extendían por los cuerpos, alcanzando un equilibrio en el que todos los cuerpos en contacto contenían la misma cantidad de calor, tal y como lo podía atestiguar un termómetro.
De hecho los termómetros cada vez más precisos permitieron a los filósofos medir incluso aquello que no entendían. Por ejemplo, la mezcla de dos muestras de agua a diferentes temperaturas iniciales y la medición de la temperatura de la mezcla abordaba una cuestión que interesaba a los médicos desde los tiempos de Galeno: si dos cosas poseen la misma cualidad en diferentes grados, ¿cuál es el grado de la cualidad cuando se mezclan?

Según unas mediciones realizadas en 1747-48 por el académico de San Petersburgo Georg Wilhelm Richmann (tristemente famoso porque murió intentando repetir el experimento de Franklin con el rayo) la temperatura T de la mezcla es
T = (m1T1 + m2T2) / (m1 + m2),
donde los subíndices denotan las temperaturas y las cantidades de las dos muestras antes de mezclarse. La fórmula insinúa la conservación del calor y mide la cantidad de calor (q) como el producto de la masa por la temperatura.

Daniel Gabriel Fahrenheit fue quizás el primero en advertir que el asunto del calor era mucho más interesante de lo que la fórmula de Richmann dejaba entrever. Fahrenheit observó que al agitar agua superenfriada (esto es, a una temperatura por debajo de la de fusión pero aún líquida) ésta se convertía en hielo y aumentaba su temperatura a 32 grados de su escala particular (equivalente 0º Celsius). También observó que el mercurio presentaba un efecto menor en los experimentos de mezcla que una cantidad igual de agua.
Joseph Black continuó estos experimentos en la década de los cincuenta del siglo XVIII y llegó a la conclusión de que el agua en el punto de congelación debía contener “calor oculto al termómetro”. Para confirmar esta idea midió el tiempo necesario para fundir la nieve, que consideró que sería proporcional a la cantidad de calor oculto o calor latente en el agua líquida a la temperatura de fusión.
Respecto a las diferencias en eficiencia entre el mercurio y el agua, Black las atribuyó a diferencias en su “capacidad para el calor”. Midió la capacidad de calor específica de una sustancia comparando los tiempos necesarios para calentar la misma cantidad de agua y de la sustancia desde una temperatura a otra: cuanto más pequeño el tiempo, menor era la capacidad (la sustancia podía “contener” menos calor y se “llenaba” antes, lo que correspondía a un aumento de la temperatura).
Black no publicó los resultados de sus experimentos, muchos de los cuales llevó a cabo en una cervecera para asegurarse un calor constante. Tampoco filosofó sobre la verdadera naturaleza del calor.
Johan Carl Wilcke llegó al concepto de calor latente en 1772 al observar que el agua caliente fundía menos nieve de lo que la fórmula de Richmann daba a entender. Diez años después Wilcke también llegó al concepto de calor específico, puede que de forma independiente a Black, cuyos datos se habían difundido por parte de sus alumnos y colegas. Wilcke, a diferencia de Black, sí publicó sus ideas, entre las que se encontraba que el el calor era un fluido elástico del mismo estilo que la electricidad.
Los filósofos naturales aceptaron rápidamente los conceptos de calor latente y calor específico, mientras que los químicos introdujeron una nueva clase de combinación para explicar la presencia de calor “ligado” que no actúa sobre el termómetro.
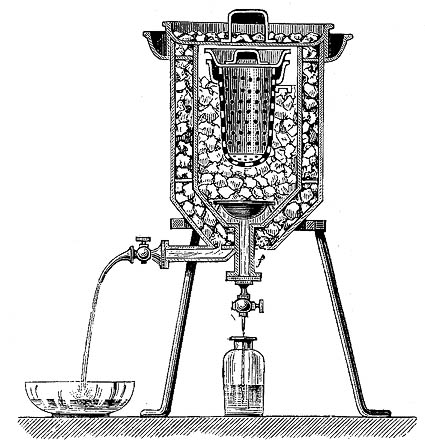
Antoine-Laurent Lavoisier se basó en estas ideas para definir una “materia del fuego” que se liberaba durante la combustión y la calcinación y que daba lugar a los estados líquido y gaseoso. Lavoisier y el matemático Pierre-Simon de Laplace diseñaron un método en los primeros años ochenta del XVIII para medir las cantidades de materia del fuego liberadas durante los procesos físicos y químicos mediante la cantidad de hielo que se fundía cuando el proceso en cuestión tenía lugar en un entorno cerrado que se mantenía a la temperatura del hielo en fusión. Con el tiempo terminaron llamando al aparato calorímetro y renombrarían a la materia del fuego como calórico. Esta nueva nomenclatura apenas ocultaba la procedencia de su nuevo concepto rigurosamente definido de las ideas antiguas sobre la naturaleza del fuego.

A la vuelta del siglo la cuestión se centraba en la relación entre el calórico, el fuego, el calor y los rayos caloríficos (calor radiante) descubiertos por William Herschel en 1800. Incluso después de que Benjamin Thompson (el conde Rumford) demostrase en la última década del XVIII que se podía obtener una cantidad ingente de calor de una masa metálica cuando se la horadaba para convertirla en un cañón, la inmensa mayoría de los filósofos naturales y químicos aún pensaban que el calor era algo material y lo asimilaban al calórico. ¿Pudiera ser que el fuego no fuese más que calórico con partículas de luz?
Con la sustitución de la teoría corpuscular de la luz por la ondulatoria en los años veinte y treinta del XIX y la aceptación de la teoría cinética de los gases en los cuarenta y cincuenta la cuestión se resolvió por sí misma. Los químicos y físicos (el término físico fue creado en 1840 por William Whewell para sustituir al de filósofo natural) llegaron al acuerdo de que las materias del fuego, el calor y la luz eran la misma, en el sentido de que ninguna de ellas existía.
Este post ha sido realizado por César Tomé López (@EDocet) y es una colaboración deNaukas con la Cátedra de Cultura Científica de la UPV/EHU.
Nota del autor: Este texto, y en especial la coda final, está dedicado con afecto al físico experimental Javier Fernández Panadero.


Lo Mejor de la Semana (31 de mayo – 6 de junio) | Hablando de Ciencia | Artículos
[…] Fuego y calor, esas materias inexistentes. La naturaleza última de dos fenómenos físicos omnipresentes, el fuego y el calor, desconcertó a los filósofos naturales hasta mediados del siglo XIX. La pregunta de si el agente del calor, que podía funcionar sin emitir luz, era diferente de la causa del fuego, al que los antiguos habían dado estatus de elemento fundamental de todo lo existente, se convirtió en insistente a finales del XVIII. […]
Hitos en la red #71 – Naukas
[…] materia del fuego o del calor (aunque no sé yo que diría la población general en una encuesta), Fuego y calor, esas materias inexistentes, como siglos se han necesitado para abandonar los métodos mecánicos de cálculo, El primer […]