Trasplante de mitocondrias, mitocondriopatías y Parkinson
Los seres vivos eucariotas producen normalmente la energía que necesitan oxidando moléculas orgánicas en una especie de combustión finamente regulada. El proceso de oxidación es realizado por las mitocondrias (Figura 1), unos orgánulos celulares cuyo origen es fascinante. Las mitocondrias se originaron por un fenómeno de simbiosis entre una bacteria hospedadora y bacterias capaces de realizar la oxidación de sustratos. Esta simbiosis, junto con la formación de un núcleo definido, está en el origen de las células eucariotas.
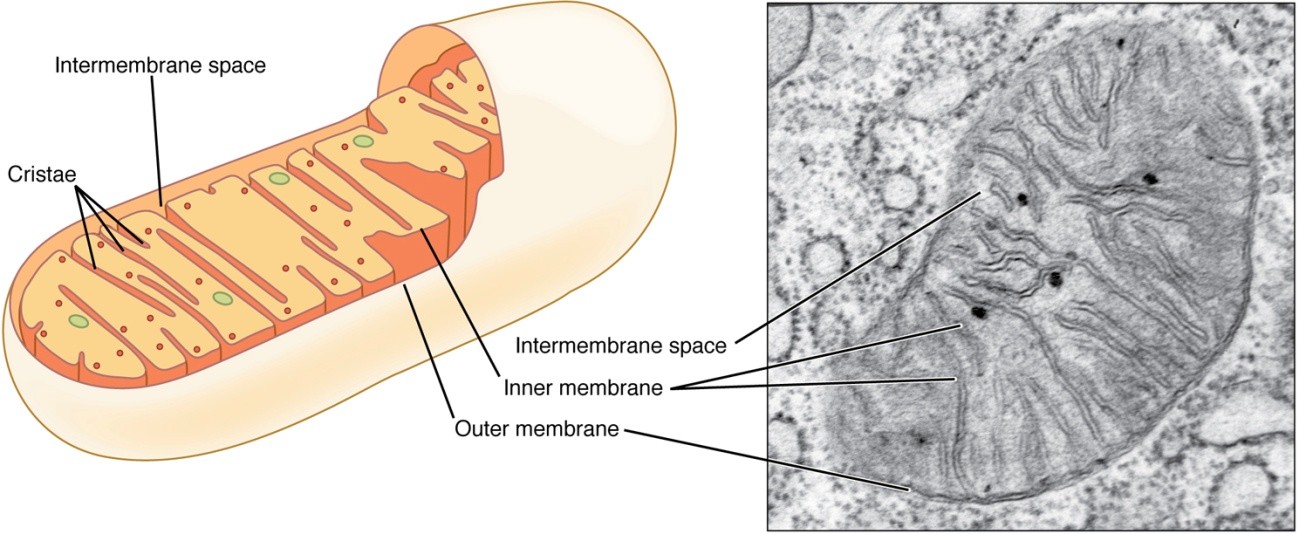
Las mitocondrias mantienen rasgos de este origen ancestral bacteriano. Por ejemplo, se reproducen por división y contienen una cadena circular de ADN que, en humanos, codifica 37 genes funcionales. Sin embargo, muchos genes necesarios para la función mitocondrial están en el núcleo celular, por lo que las mitocondrias ya no pueden vivir independientemente como hacían sus antecesoras bacterianas.
Dado que las mitocondrias son las centrales energéticas de las células, su mal funcionamiento tiene consecuencias que pueden ser muy graves. Estas patologías se denominan mitocondriopatías, y normalmente se deben a mutaciones, bien en el ADN mitocondrial o en los genes nucleares relacionados con la función mitocondrial. Se trata de enfermedades raras, con una incidencia de un caso por cada 5000 humanos. Entre las más importantes están los síndromes MELAS, MERRF y Leigh. La deficiente producción energética debida al mal funcionamiento de las mitocondrias produce daños severos en el sistema nervioso, corazón, músculos o hígado, grandes consumidores de energía.
El tratamiento de las mitocondriopatías suele ser sintomático, pero hay esperanzas de que la terapia génica pueda reparar en el futuro las mutaciones que las causan. Otra interesante opción es reemplazar las mitocondrias dañadas por mitocondrias sanas, no afectadas por las mutaciones. El problema es fundamentalmente técnico, ya que es necesario insertar mitocondrias sanas en las células afectadas y esto no resulta sencillo. Hasta ahora se han intentado diferentes procedimientos, por ejemplo inyectar directamente mitocondrias aisladas en las proximidades de las células objetivo, pero la eficiencia de esta técnica es muy baja.
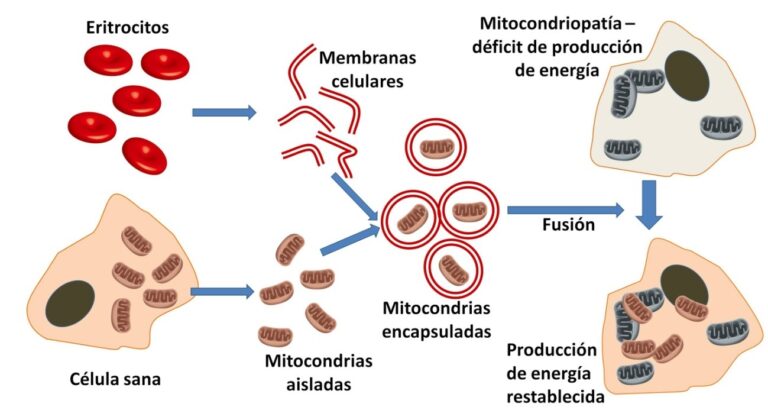
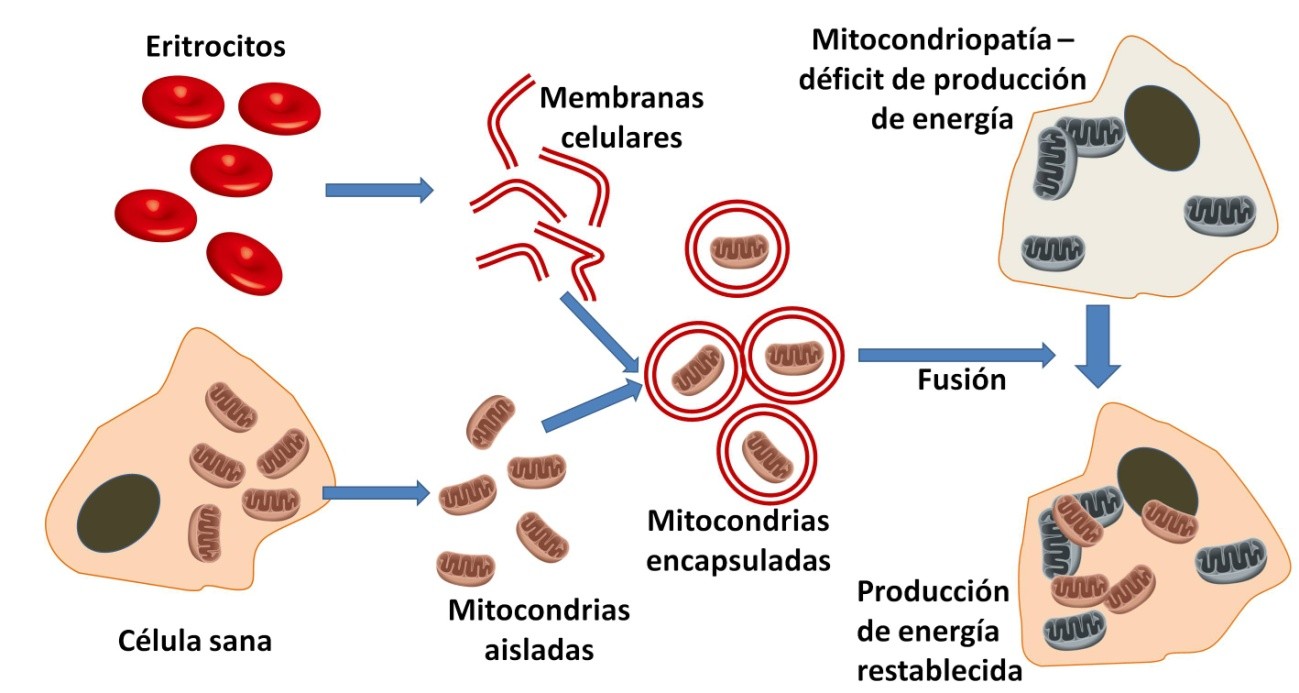
Por este motivo resulta del mayor interés el artículo recién publicado en Cell por un grupo de científicos chinos, en el que describen una técnica de trasplante de mitocondrias con una eficiencia no lograda hasta ahora. El método consistió en aislar mitocondrias sanas y encapsularlas en membranas derivadas de glóbulos rojos. De esta forma se obtienen vesículas de alrededor de una micra de diámetro, con tendencia a fusionarse con las células y liberar al citoplasma la mitocondria transportada (Figura 2). En sucesivos experimentos, el grupo demostró una alta eficiencia del trasplante en cultivos de células de ratón y de primate. Además, células procedentes de un modelo de ratón con mitocondriopatía recuperaron la capacidad normal de producir energía tras el trasplante.
El modelo que hemos mencionado consiste en ratones deficientes en el gen Ndufs4, que codifica una proteína de la cadena de transporte de electrones mitocondrial[1]. Este es uno de los genes cuya mutación en humanos produce el síndrome de Leigh. Se trata de una enfermedad mitocondrial neurodegenerativa que afecta principalmente a lactantes, provocando regresión psicomotora, hipotonía, dificultades de alimentación y problemas respiratorios. El déficit de energía en el sistema nervioso causa una alta mortalidad, y actualmente no existe una tratamiento curativo. Los ratones con deficiencia del gen Ndufs4 reproducen los síntomas del síndrome de Leigh, y por eso son un buen modelo para ensayar terapias.
En 2024, un equipo japonés-estadounidense probó a inyectar mitocondrias libres en la circulación de estos ratones, o trasplantar células de médula ósea sanas, que también liberan mitocondrias, a la sangre. En ambos casos se logró una mejora de las funciones neurológicas del ratón y un aumento moderado de su supervivencia. Sin embargo, el ensayo del equipo chino con mitocondrias encapsuladas mejoró estos resultados. La supervivencia media alcanzó los 74 días, frente a los 61 días que logran las mitocondrias libres o los 48 días de los ratones no tratados. No se puede hablar de curación, pero es un avance.
También se ensayó el tratamiento con mitocondrias encapsuladas en un modelo de enfermedad de Parkinson en ratón. Este experimento se basaba en un artículo publicado en 2021, en el que se describió que la disrupción de un complejo mitocondrial de proteínas en las neuronas dopaminérgicas de la sustancia negra provocaba el desarrollo de parkinsonismo. Estas neuronas inervan otras áreas del cerebro, y su degeneración produce un déficit de dopamina, causa de los síntomas del parkinsonismo. De nuevo, la inyección de mitocondrias encapsuladas en un modelo de ratón, tanto por vía intravenosa como directamente en la sustancia negra cerebral, produjo una clara mejoría de los síntomas. Se observó un aumento de la inervación dopaminérgica, un incremento en los niveles de la tirosina hidroxilasa, enzima clave en la síntesis de dopamina, y una mayor movilidad. La recuperación se extendió más allá de los tres meses y superó con creces a los tratamientos con mitocondrias aisladas.
El desafío que supone el trasplante de mitocondrias no se ha resuelto, ni mucho menos, pero los avances en este campo permiten atisbar esperanzas de que las mitocondriopatías puedan tener un tratamiento eficaz.
Referencias
Du, S., Long, Q., Zhou, Y. et al. (2026) Transplantation of encapsulated mitochondria alleviates dysfunction in mitochondrial and Parkinson’s disease models Cell doi: 10.1016/j.cell.2026.02.023
Sobre el autor: Ramón Muñoz-Chápuli Oriol es Catedrático de Biología Animal (jubilado) de la Universidad de Málaga.
Nota:
[1] La cadena de transporte de electrones es una serie de complejos proteicos que se encuentran en la membrana interna mitocondrial. Mediante reacciones bioquímicas producen trifosfato de adenosina (ATP) que es el compuesto energético que utilizan los seres vivos.