Las bacterias cable, conductores eléctricos vivientes
La forma usual en que los seres vivos obtienen energía de la materia orgánica es mediante la respiración celular. En este proceso se oxidan moléculas como glucosa, lípidos o proteínas para obtener ATP, la molécula energética básica de la célula. Excepto en las bacterias, este proceso se desarrolla en las mitocondrias. Básicamente, las moléculas orgánicas son procesadas para producir dióxido de carbono, protones (núcleos de hidrogeno cargados positivamente) y electrones. Los electrones son transportados a través de una serie de proteínas que constituyen la cadena respiratoria, y el ATP se genera a lo largo de este proceso. Finalmente los electrones son traspasados a un aceptor, oxígeno en el caso del metabolismo aeróbico. La combinación de dos electrones con dos protones y un átomo de oxígeno culmina el proceso formando una molécula de agua.
En las bacterias, la obtención de energía implica también generalmente un transporte de electrones, aunque encontramos mucha variabilidad en lo que se refiere a los donadores y aceptores de electrones. Los mecanismos de transporte también son variados, aunque siempre compuestos por proteínas que actúan en el interior de cada bacteria y en distancias muy cortas (nanómetros, es decir, millonésimas de milímetro). Sin embargo, en 2010 se descubrió un insólito sistema bacteriano de transporte de electrones a largas distancias (centímetros). Hablamos de las “bacterias cable”, concretamente de los géneros Electronema y Electrothrix, de la familia Desulfobulbáceas.

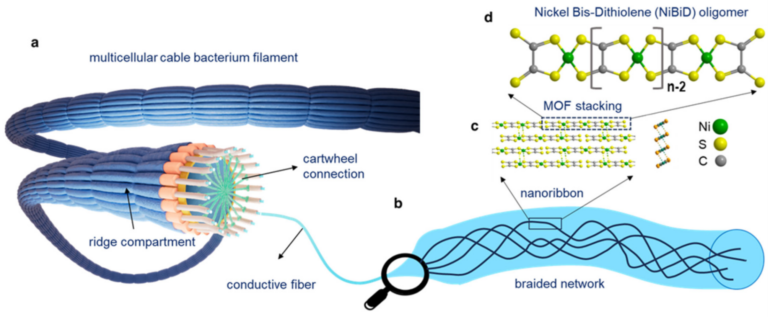
Las bacterias cable utilizan sulfuro de hidrógeno (H2S)[1] como sustrato energético y donador de electrones. Otras bacterias también oxidan H2S para producir energía, pero las bacterias cable lo hacen de una forma especial. En determinados fondos marinos o dulceacuícolas, el H2S se acumula en el sustrato a una cierta profundidad, sin oxígeno disponible. Esto haría imposible la oxidación del H2S, pero las bacterias cable resuelven el problema de forma original. Cada una de ellas mide unas tres micras (milésimas de milímetro), pero se agrupan por decenas de miles en largos filamentos, de más de un centímetro de longitud (Figura 1). Un extremo del filamento se hunde en el sustrato sin oxígeno, y las bacterias de ese extremo convierten el sulfuro en sulfato utilizando agua y protones (Figura 1). La cuestión es cómo conducir los electrones liberados en la reacción hasta la zona que contiene oxígeno, el aceptor de electrones como antes dijimos.
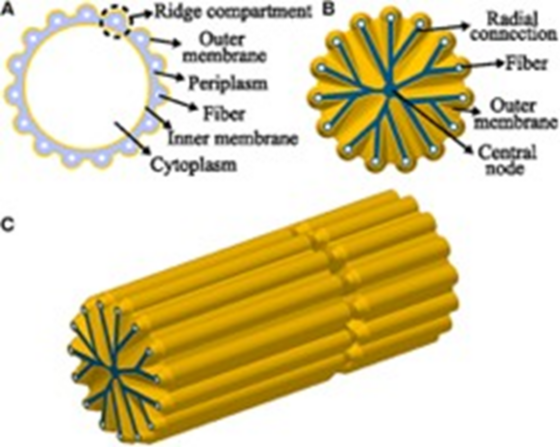
Utilizando técnicas de microscopía electrónica se descubrió que estas bacterias están rodeadas por dos membranas, la interna, propia de cada célula, y la externa, común a todo el filamento. Entre ellas hay un espacio denominado periplasma, que está recorrido por 15-60 fibras finísimas (50 nanómetros de diámetro). Entre cada dos células existe una estructura en forma de rueda de carro, rica en cobre, que conecta las fibras de bacterias contiguas (Figura 2). Las medidas hechas sobre los filamentos bacterianos revelaron que eran excelentes conductores de electricidad, lo que permitía trasladar electrones desde la zona profunda a la zona oxigenada. Este transporte colectivo de electrones se produce a distancias millones de veces mayores que las que operan a nivel de las mitocondrias.
En 2021, un estudio estableció que las nanofibras superficiales estaban formadas por proteína, azufre y níquel. Esto fue una sorpresa ya que el níquel solo es utilizado por unas pocas enzimas no relacionadas con el transporte de electrones, fenómeno que sí implica frecuentemente al hierro o al cobre asociados a proteínas.
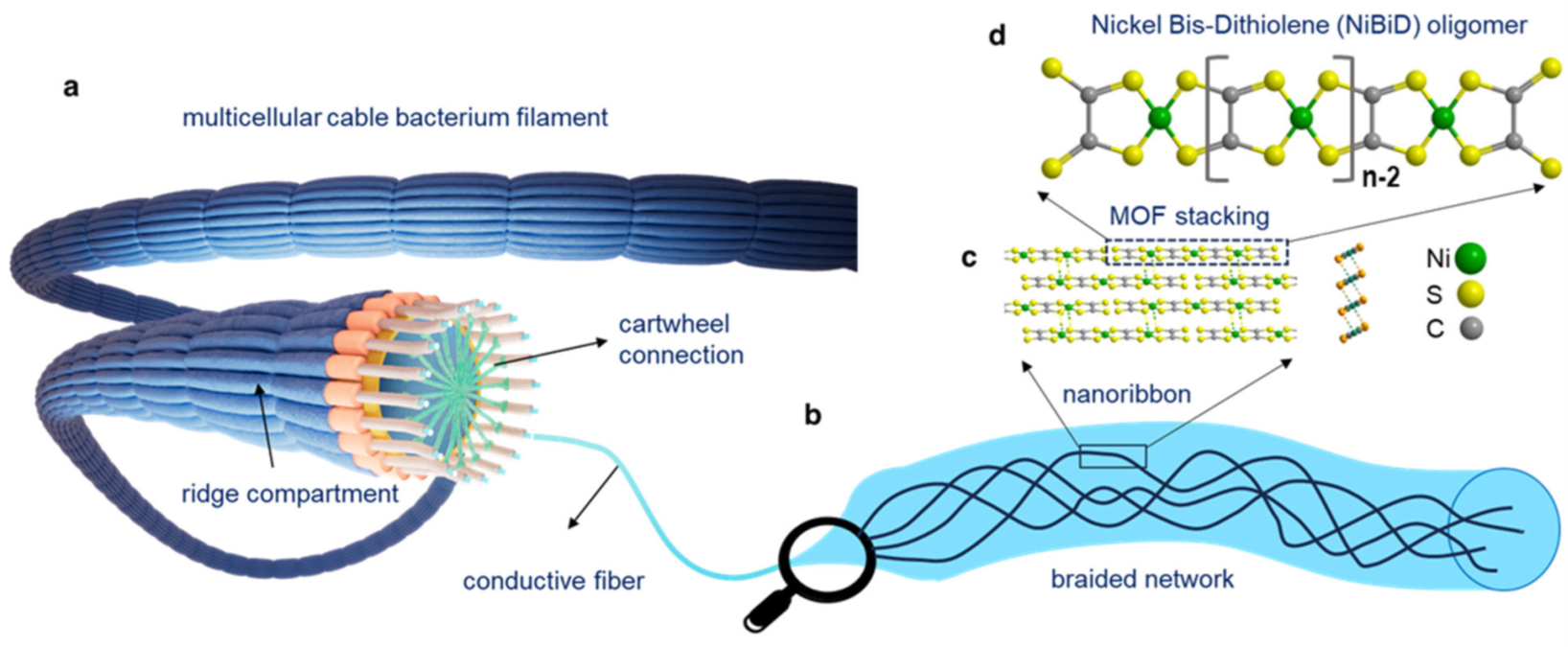
Lo que seguía siendo una incógnita, hasta ahora, era cómo el níquel se organiza en el seno de las fibras para conducir la electricidad. Un grupo de investigación belga-neendarlés, pionero en el estudio de las bacterias cable, acaba de publicar la respuesta en BioRxiv[2]. El níquel se encuentra integrado en una molécula de níquel bis(dithioleno) (NiBiD), donde conecta con cuatro átomos de azufre que, a su vez, se unen a átomos de carbono. Repeticiones de esta molécula forman unas “nanocintas” conductoras que se integran en el núcleo de las fibras que recorren el periplasma (Figura 3). Las proteínas que rodean ese núcleo actúan como aislantes, exactamente igual que en los cables eléctricos.
NiBiD es un compuesto organometálico, y esta es la primera vez que una configuración de este tipo aparece implicada en un proceso fisiológico. Curiosamente, el Premio Nobel de Química 2025 ha sido otorgado a Susumu Kitagawa, Richard Robson y Omar M. Yaghi por el desarrollo de las estructuras organometálicas, compuestas por iones metálicos y moléculas orgánicas. El interés que existe hacia este tipo de estructuras es enorme por sus múltiples aplicaciones en ingeniería o electrónica. Como afirman los autores de la investigación, resulta llamativo que poco después de la concesión del Nobel, unas bacterias nos recuerden que ellas ya usaban estos compuestos hace millones de años.
¿Tendrá este sorprendente descubrimiento aplicaciones en bioingeniería? Es probable que sí, dado que los materiales biológicos suelen ser malos conductores de la electricidad. Por ejemplo, puede pensarse en la fabricación de dispositivos electrónicos biodegradables o implantes terapéuticos biocompatibles y reabsorbibles por el organismo.
Referencias
Meysman, F.J.R., Smets, S., Hidalgo-Martinez, S. et al. (2025) A hierarchical nickel organic framework confers high conductivity over long distances in cable bacteria. BioRxiv 2025.10.10.681601; doi: 10.1101/2025.10.10.681601.
Notas:
[1] También llamado ácido sulfhídrico, el componente fundamental del olor a huevos podridos.
[2] Se trata de un repositorio de acceso abierto en el que se pueden depositar manuscritos antes de su evaluación por pares y su eventual publicación en revistas científicas.
Sobre el autor: Ramón Muñoz-Chápuli Oriol es Catedrático de Biología Animal (jubilado) de la Universidad de Málaga.