En The Big Bang Theory no hay químicos, sin embargo…

En la serie The Big Bang Theory hay físicos, biólogos, ingenieros… pero no hay ningún personaje protagonista que sea químico. Sheldon Cooper es físico teórico, Leonard Hofstadter es físico experimental, Raj Ramayan Koothrappali es astrofísico, Howard Wolowitz es ingeniero mecánico, Bernardette Rostenkowski es microbióloga, Amy Farrah Fowler es neurobióloga y Penny es una aspirante a actriz que, siendo la única protagonista sin formación científica, acaba trabajando como visitadora médica.
En el último capítulo emitido, el episodio 13 de la temporada 11, Leonard y Amy juegan en casa a reproducir algunos de los experimentos que hicieron en sus años de colegio. El primero de ellos es un experimento de química. Ninguno de los dos es químico, sin embargo, deciden hacer un experimento de química para obtener «hielo caliente».
-We’re making «hot ice».
-It’s very cool!
El «hielo caliente»no es realmente hielo, es decir, no se trata de agua sólida a una temperatura diferente a los cero grados Celsius, sino que se trata de otro sólido que, a simple vista, se parece mucho al hielo.
Lo sorprendente de este experimento es que, al introducir la mano u otro objeto en un vaso que parece contener agua, éste se recubre instantáneamente con algo similar a cristales hielo. Es muy bonito y aparente, por eso es un experimento al que se recurre con frecuencia en las clases de química del instituto.

No son cristales de hielo, sino que son cristales de acetato de sodio. Podemos comprar el acetato de sodio, en cambio, también podemos sintetizarlo en casa con dos sustancias que habitualmente todos tenemos en nuestra cocina: vinagre blanco, el mismo que usamos para las ensaladas, y bicarbonato, lo que utilizamos para que los bizcochos luzcan esponjosos —y para un montón de cosas más—.
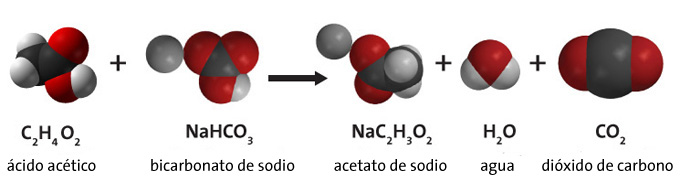
El vinagre es una disolución de ácido acético en agua. El bicarbonato es una sal, el hidrogenocarbonato de sodio. Si echamos un par de cucharadas de bicarbonato sobre medio litro de vinagre estaremos dando el primer paso para producir acetato de sodio. Lo que observaremos es una reacción química muy efervescente. Se forman cientos de pequeñísimas burbujas, como cuando agitamos enérgicamente una bebida gaseosa. Lo que está ocurriendo es que los átomos de ambos compuestos se reordenan para dar lugar a nuevos compuestos más estables. Esta es la definición de reacción química. En este caso forman acetato de sodio, agua y dióxido de carbono. El dióxido de carbono es el gas que observamos como burbujas.
 Lo que nos interesa para hacer «hielo caliente» es el acetato de sodio. Tenemos que reducir la cantidad de agua y de dióxido de carbono producidos y forzar a que todo el ácido acético reaccione efectivamente con el bicarbonato. El dióxido de carbono es el menor de nuestros problemas, ya que el ser un gas, se escapa por sí solo. Para el resto, lo más efectivo es calentar la mezcla hasta que hierva. Al hervirla estamos evaporando gran parte del agua que se produjo, de modo que, por un lado, forzamos a que todo reaccione y, por otro lado, cuanta menos agua más saturada estará la disolución de acetato resultante.
Lo que nos interesa para hacer «hielo caliente» es el acetato de sodio. Tenemos que reducir la cantidad de agua y de dióxido de carbono producidos y forzar a que todo el ácido acético reaccione efectivamente con el bicarbonato. El dióxido de carbono es el menor de nuestros problemas, ya que el ser un gas, se escapa por sí solo. Para el resto, lo más efectivo es calentar la mezcla hasta que hierva. Al hervirla estamos evaporando gran parte del agua que se produjo, de modo que, por un lado, forzamos a que todo reaccione y, por otro lado, cuanta menos agua más saturada estará la disolución de acetato resultante.
Si lo dejamos hervir el tiempo suficiente, veremos cómo se empieza a formar una película superficial. Esto nos indica que la disolución está suficientemente concentrada (estará sobresaturada), así que la apartamos del fuego y la dejamos enfriar. Una vez fría, la dejamos refrigerar media hora en la nevera.
Si a continuación introducimos cualquier objeto o nuestra mano en esa disolución, ¡sorpresa!, empezarán a crecer cristales a su alrededor inmediatamente. Esto es lo que hacen Leonard y Amy, introducir una varilla metálica en la disolución. Ésta se empieza a cubrir de cristales. En la serie hacen un primer plano del suceso, así que en este capítulo se observa muy bien la cristalización.

Lo que está ocurriendo es que el acetato de sodio está sobreenfriado. Se mantiene en estado líquido aunque esté por debajo de su temperatura de fusión (54oC). Este estado es inestable, por lo que cualquier perturbación —como introducir un objeto— desencadena que las moléculas de acetato comiencen a organizarse formando cristales, que es su estado estable a temperatura ambiente. Al ser un proceso tan favorable, sucede desprendiendo calor. A esto se le denomina proceso exotérmico. Es decir, la disolución se calienta a medida que se produce la cristalización. Por eso al meter la mano no solo sentimos cómo se forman cristales, sino que también sentiremos cómo estos se calientan, de ahí el nombre de «hielo caliente».
Por el momento no hay químicos en la serie The Big Bang Theory, como tampoco están representados científicos de otras muchas áreas de la ciencia. Sin embargo, han sido el físico experimental y la neurobióloga los que se han puesto a jugar a las cocinitas y a darle un poco a esa maravillosa ciencia llamada química.
Sobre la autora: Déborah García Bello es química y divulgadora científica

Afotoquimico
Lo que está ocurriendo es que el acetato de sodio está sobreenfriado. Se mantiene en estado líquido aunque esté por debajo de su temperatura de fusión (54°C).
Esto, aunque se entienda lo que quiere decir, no es correcto. El punto de fusión del acetato sódico es de más de 300°C.
Hitos en la red #200 | Enlace Recomendado | Naukas
[…] En The Big Bang Theory no hay químicos, sin embargo… […]
Ana
Todo el día intentando hacer el experimento con mi hijo de 11 años… y no sé qué estamos haciendo mal :-)) Se nos ha solidificado la mezcla después de dejarla hervir… Si es que yo soy de letras, no sé como me meto en estos fregados…
QUIMIKOLOKO
Afotoquimico, lo correcto es decir que la «DISOLUCION de acetato de sodio esta subenfriada» es decir, a esa temperatura deberia de haber precipitado el solido. Nada tiene que ver con su punto de fusion.
Ana, prueba a filtrar la disolucion antes de enfriarla, no debe quedar ni una mota de solido cuando la metas al frigo, de lo contrario, el solido empieza a formarse alrededor de esa mota. En teoria tambien ayudria que utilizases un recipiente nuevo y sin arañazos.
Suerte 😉
sonia argente
Muchas gracias por tus explicaciones tan minuciosas, me sirve para práctica de Secuandaria.
Un saludo
En The Big Bang Theory no hay químicos, sin embargo… | Deborah Ciencia
[…] Seguir leyendo en #Fronteras en el Cuaderno de Cultura Científica de la UPV/EHU>> […]