La enfermedad del hígado graso no alcohólico, una gran desconocida
Jenifer Trepiana, Saioa Gómez-Zorita, María P. Portillo, Maitane González-Arceo
La enfermedad del hígado graso no alcohólico (EHGNA) consiste en una acumulación excesiva de grasa en las células del hígado o hepatocitos (más del 5% del peso del hígado sería grasa) sin un consumo excesivo de alcohol, siendo en la actualidad la causa más frecuente de enfermedad hepática (Ahmed, 2015). Puede presentarse como esteatosis (acumulación de grasa) simple o como esteatohepatitis, situación de mayor gravedad que comporta ya inflamación y un inicio de fibrosis.
La prevalencia de la esteatosis simple oscila entre un 14% y un 30% en la sociedad occidental, aunque es probable que sea mayor ya que como muchos pacientes son asintomáticos, en ocasiones no son diagnosticados (Abd El-Kader SM y El-Den Ashmawy EM, 2015).
¿Cómo se desarrolla la EHGNA?
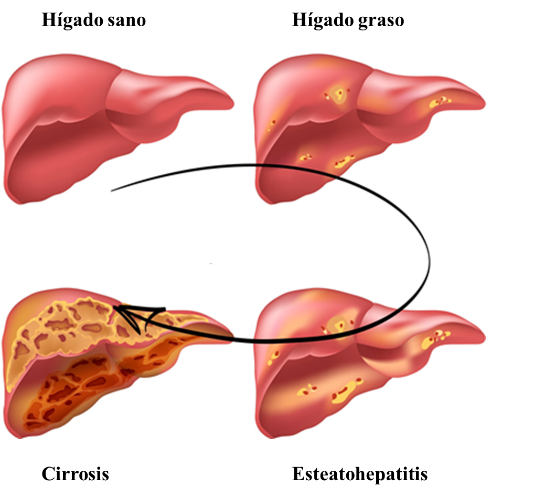
El hígado graso no alcohólico comprende numerosas lesiones hepáticas, comenzando con la esteatosis simple, que supone el 80-90% de los casos. Hay que destacar que el hígado graso no alcohólico se desarrolla de una manera progresiva y lenta, siendo la esteatosis simple reversible, y pudiendo dejar de progresar. Sin embargo, en el 10-20% de los pacientes avanza hasta la siguiente etapa llamada esteatohepatitis o inflamación del hígado. De la misma manera, la esteatohepatitis puede no seguir progresando o, por el contrario, puede evolucionar mediante la aparición de fibrosis a su etapa final, llamada cirrosis, con riesgo de desarrollar carcinoma de hígado en el peor de los casos (Hashimoto et al., 2013).
Lo que ocurre en la esteatosis simple, es que la excesiva acumulación de lípidos en el hígado lo hace vulnerable a otras agresiones como el estrés oxidativo, provocado por un desequilibrio entre los radicales libres y la disponibilidad de antioxidantes, además de promover la liberación de moléculas que producen inflamación provocando esteatohepatitis. En la esteatohepatitis, aparece inflamación y daño en las células de manera crónica que puede cursar con fibrosis (formación excesiva de un tejido llamado tejido conectivo para intentar reparar la víscera). Según estudios científicos, un 41% de los pacientes que sufren la EHGNA desarrollan fibrosis (Ekstedt et al., 2006). Por otra parte, el riesgo de padecer hepatocarcinoma en los pacientes con EHGNA que no sufren cirrosis es mínimo (de 0-3% en 20 años), mientras que en pacientes con cirrosis el riesgo asciende a 12,8% en 3 años (White et al., 2012).
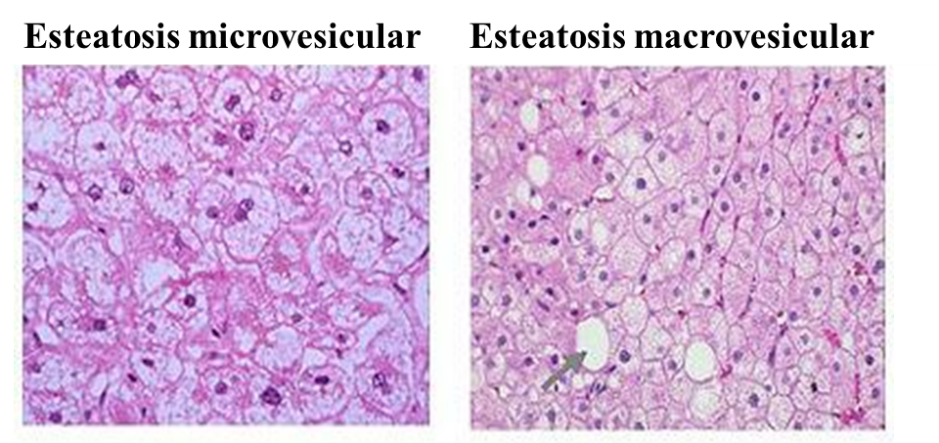
Al analizar la morfología del hígado de pacientes que sufren EHGNA tras una biopsia, se observa una acumulación de grasa en las células del hígado (hepatocitos) en forma de triglicéridos. Se ha aceptado que el criterio mínimo para diagnosticar la EHGNA mediante el estudio con microscopía de este órgano, es que el hígado contenga una cantidad mayor al 5% de hepatocitos esteatóticos (Neuschwander-Tetri y Caldwell, 2003), es decir que más de un 5% de las células del hígado contengan una gran cantidad de grasa en su interior. Así, mediante estas técnicas de imagen, se puede clasificar la EHGNA en diferentes tipos, desde una esteatosis simple, hasta esteatohepatitis con o sin fibrosis.
Centrándonos más en lo que le ocurre al hepatocito, podemos decir que normalmente, la esteatosis en el hígado graso no alcohólico, es de tipo macrovesicular. Esto es, que el hepatocito contiene una única gota grande de grasa, o varias gotas de grasa algo más pequeñas, lo que provoca el desplazamiento del núcleo de la célula a la periferia (extremos) del hepatocito. Sin embargo, en la esteatosis de tipo microvesicular, el núcleo se mantiene en el centro del hepatocito con diminutas gotículas de grasa presentes en la célula (Brunt y Tiniakos, 2010). Este último tipo, no suele ser la forma más típica de esteatosis, encontrándose sobre todo en los hepatocitos más pequeños o en los que no se encuentran en las zonas donde la esteatosis es más prominente. Cuando se da esta situación, el paciente suele tener peor pronóstico. En alguna ocasión, también puede ocurrir que se produzca una esteatosis mixta, donde se encuentran hepatocitos con una esteatosis macrovesicular, a la vez que encontramos grupos de hepatocitos con esteatosis microvesicular.
¿Qué factores influyen en el desarrollo de esta enfermedad?
El origen de la EHGNA no está claro, aunque probablemente sea la resistencia a la insulina la causa principal. Otros factores de riesgo asociados con el hígado graso son el sobrepeso y la obesidad, la dislipemia (altos niveles de colesterol y/o triglicéridos en sangre), y la diabetes mellitus tipo 2. Hay que tener en cuenta que la EHGNA afecta a todos los segmentos de la población, no solo a los adultos, y también a la mayoría de los grupos raciales. Se estima que entre el 74% y el 80% de los individuos obesos presentan hígado graso. Además de la obesidad, la presencia de diabetes mellitus tipo 2 incrementa no solo el riesgo, sino también la severidad de la EHGNA (Angulo, 2002). Esto quiere decir, que la diabetes mellitus tipo 2 constituye un perfil metabólicamente desfavorable para los pacientes que presentan EHGNA, aumentando el riesgo de sufrir enfermedades cardiovasculares.
¿Cómo se detecta la EHGNA?
Como hemos indicado al inicio, con mucha frecuencia, la EHGNA cursa de manera asintomática, y cuando produce síntomas estos son bastante inespecíficos. Por ello, muchas veces pasa desapercibida, tanto para los médicos como para los pacientes. El síntoma más frecuente es dolor en la zona abdominal derecha y fatiga.
Para la detección de la EHGNA, primeramente se suelen valorar las transaminasas hepáticas (AST, aspartatoaminotransferasa y ALT, alaninaaminotransferasa), que se suelen encontrar aumentadas. No obstante, aunque los niveles de transaminasas son lo primero que se analiza mediante una extracción de sangre del paciente, no son consideradas buenos marcadores ya que en algunos individuos con esteatosis los niveles de transaminasas en sangre no están elevados, incluso en algunos pacientes con cirrosis tampoco lo están. Además, solo pueden indicar daño hepático en general, no siempre teniendo que ir asociado a la EHGNA. Por otro lado, la AST aparece en otros tejidos como el corazón o el músculo esquelético, por lo que en caso de que se eleve, también puede deberse a una alteración en otros órganos o tejidos. También se recurre a técnicas de imagen para ayudar en el diagnóstico de la enfermedad o para la detección de hepatomegalia (hígado más grande de lo normal), como son la ecografía, TAC (Tomografía Axial Computarizada) o RMN (Resonancia Magnética), siendo esta última la más eficaz en su diagnóstico. Estas pruebas de imagen son útiles para saber si hay infiltración de grasa en el hígado, pero presentan la limitación de que no muestran si el hígado presenta inflamación o fibrosis.
Por ello, el mejor método de diagnóstico es la biopsia, que además permite conocer el grado de EHGNA del paciente. No obstante, dado que se trata de una técnica invasiva, únicamente se suele realizar en aquellos pacientes que muestran signos de estar en un estadio avanzado de enfermedad hepática (por ejemplo, cirrosis) o en aquellos pacientes que presentan mayor probabilidad de esteatohepatitis. Una limitación de esta técnica es que las lesiones hepáticas sufridas no son uniformes en todo el hígado, lo que dificulta el análisis de las biopsias. Es decir, según de qué zona del hígado se tome la muestra, el diagnóstico puede variar.
Ante la necesidad de detectar la EHGNA sin tener que recurrir a la biopsia hepática, se está profundizando en el estudio de biomarcadores para analizar la función hepática de una manera no agresiva para el organismo. Entre ellos encontramos marcadores específicos para la fibrosis, como la medición de concentraciones de proteínas implicadas en la fibrolisis o rotura del tejido fibrótico (colagenasas, α2-macoglobulina, MMPs, C3M) o de proteínas que participan en la fibrogénesis o generación del tejido fibrótico (colágeno tipo IV, pro-C3/C5). En la práctica clínica se suelen utilizar diversos test como el SteatoTest que calcula el grado de esteatosis hepática en pacientes con riesgo metabólico elevado, el FibroTest que valora los niveles de fibrosis y cirrosis, así como el grado de inflamación del hígado, y el NashTest que predice la presencia o ausencia de esteatohepatitis. Los marcadores que se analizan mediante estos tests son la α2-macroglobulina, haptoglobina, apolipoproteína A1, bilirrubina total, ALT, GGT, glucosa en ayunas, triglicéridos, y colesterol. Estos parámetros se ajustan a la edad, sexo, peso y tamaño del paciente. Estos índices y biomarcadores pueden ser útiles no solo para el diagnóstico de la enfermedad, sino también para estudiar la evolución de esta y los efectos del tratamiento.
¿Qué se puede hacer para prevenir la EHGNA?
Es importante remarcar que para la prevención de la EHGNA la principal medida es evitar los factores de riesgo asociados a la enfermedad (obesidad, dislipemia, resistencia a la insulina). Para ello son esenciales una rutina de ejercicio físico en nuestro día a día y llevar una dieta equilibrada.
Tratamientos en la actualidad
Actualmente, no existe un tratamiento específico para la EHGNA. Por ello, lo que se suele hacer es tratar los factores causales, es decir, la obesidad, y otros componentes del síndrome metabólico, como son la hipertensión (mediante el tratamiento farmacológico con estatinas), la diabetes mellitus y la dislipemia. Al igual que en el caso de la prevención, una dieta equilibrada y la actividad física serán los pilares básicos para tratar el hígado graso no alcohólico.
Además, se ha comprobado que seguir un patrón de alimentación mediterráneo se asocia con una menor probabilidad de presentar esteatosis y esteatohepatitis (Aller et al., 2015).
Recomendaciones en el estilo de vida
-
Pérdida de peso: 3-5% en la esteatosis simple y 7-10% en la esteatohepatitis (Jeznach-Steinhagen et al., 2019).
-
Reducción del consumo de hidratos de carbono simples (< 10%), como glucosa y especialmente fructosa, ya que es un potente inductor del desarrollo de EHGNA (Mager et al., 2015).
-
Reducción de la grasa saturada de la dieta. Una dieta rica en grasas saturadas, intensifica el estrés oxidativo en el organismo, aumentando la inflamación en la zona afectada por la esteatosis. Sin embargo, el consumo de ácidos grasos poliinsaturados del grupo n-3 (omega 3) mejora la esteatosis hepática (Dasarathy et al., 2015).
-
Aumento del consumo de antioxidantes, presentes en altas cantidades en frutas y verduras.
-
Evitar la cantidad de alcohol ingerida. Dado que un abuso del alcohol provoca un desarrollo rápido de la enfermedad, se recomienda la abstinencia del alcohol.
Tratamientos farmacológicos
Como se ha mencionado anteriormente, algunos tratamientos farmacológicos están dirigidos a reducir las enfermedades asociadas al hígado graso, como son la diabetes, obesidad, y desordenes lipídicos.
-
Suplementación con vitaminas, especialmente aquellas que son antioxidantes como la vitamina E (precaución con las dosis elevadas ya que pueden tener efectos secundarios graves). Debido a la dosis empleada la vitamina E o α-tocoferol se incluye dentro de los tratamientos farmacológicos para tratar esta enfermedad.
-
Fármacos antidiabéticos: pioglitazone, rosiglitazona, liraglutide, metformina, etc. (al igual que en el caso anterior pueden tener efectos secundarios).
En la actualidad están siendo probados en diversos ensayos clínicos fármacos novedosos como el agonista del receptor Farnesoil X, o el agonista de PPARα y PPARδ (estudios en fase 2).
Referencias bibliográficas
Ahmed M. Non-alcoholic fatty liver disease in 2015. World J Hepatol. 18;7(11):1450-9 (2015).
Abd El-Kader SM, El-Den Ashmawy EM. Non-alcoholic fatty liver disease: The diagnosis and management. World J Hepatol. 28;7 (6):846-58 (2015).
Hashimoto E, Taniai M, Tokushige K. Characteristics and diagnosis of NAFLD/NASH. J Gastroenterol Hepatol. 28 Suppl 4:64-70 (2013).
Non Alcoholic Fatty Liver Disease NAFLD. Preventicum (2016).
Ekstedt M, Franzén LE, Mathiesen UL, Thorelius L, Holmqvist M, Bodemar G, Kechagias S. Long-term follow-up of patients with NAFLD and elevated liver enzymes. Hepatology. 44(4):865-73 (2006).
White DL, Kanwal F, El-Serag HB. Association between nonalcoholic fatty liver disease and risk for hepatocellular cancer, based on systematic review. Clin Gastroenterol Hepatol. 10(12):1342-1359 (2012).
Neuschwander-Tetri BA, Caldwell SH. Nonalcoholic steatohepatitis: summary of an AASLD Single Topic Conference. Hepatology. 37(5):1202-19 (2003).
Brunt EM, Tiniakos, DG. Histopathology of nonalcoholic fatty liver disease. World J Gastroenterol. 14;16(42):5286-96 (2010).
Mofrad P, Sanyal, A. Nonalcoholic Fatty Liver Disease. Medscape (2003).
Angulo P. Nonalcoholic fatty liver disease. New Engl. J. Med. 346:1221-1231 (2002).
Aller R, Izaola O, Luis DD. La dieta mediterránea se asocia con la histología hepática en pacientes con enfermedad del hígado graso no alcohólico. Nutrición Hospitalaria, 32: 2518-2524 (2015).
Jeznach-Steinhagen A, Ostrowska J, Czerwonogrodzka-Senczyna A, Boniecka I, Shahnazaryan U, Kuryłowicz A. Dietary and Pharmacological Treatment of Nonalcoholic Fatty Liver Disease. Medicina 55, 166 (2019).
Mager D, Iñiguez I, Gilmour S, Yap J, The effect of a low fructose and low glycemic index/load (FRAGILE) dietary intervention on indices of liver function, cardiometabolic risk factors, and body composition in children and adolescents with nonalcoholic fatty liver disease (NAFLD). J. Parenter. Enteral. Nutr. 39, 73–84 (2015).
Dasarathy S, Dasarathy J, Khiyami A, Yerian L, Hawkins C, Sargent R, McCullough A.J. Double-blind randomized placebo-controlled clinical trial of omega 3 fatty acids for the treatment of diabetic patients with nonalcoholic steatohepatitis. J. Clin. Gastroenterol. 49, 137–144 (2015).
Sobre las autoras:
Jenifer Trepiana1, Saioa Gómez-Zorita1,2, María P. Portillo1,2, Maitane González-Arceo1
1 Grupo de Nutrición y Obesidad. Departamento de Farmacia y Ciencias de los Alimentos. Facultad de Farmacia. Universidad del País Vasco (UPV/EHU)
2 Centro de Investigación Biomédica en Red de la Fisiopatología de la Obesidad y Nutrición (CiberObn)
La enfermedad del hígado graso no alcohólico, una gran desconocida – Blog Rocnarf
[…] Autor: Grupo de Nutrición y Obesidad. Departamento de Farmacia y Ciencias de los Alimentos. Facultad de Farmacia. Universidad del País Vasco. Julio 2019. – https://culturacientifica.com/2019/07/14/la-enfermedad-del-higado-graso-no-alcoholico-una-gran-desco… […]