Por qué se corta la mayonesa y qué relación tiene esto con la cosmética

Para hacer mayonesa se necesita aceite de oliva, vinagre, huevos y sal. Hay variantes con otros aceites, como el de girasol, o con otros ácidos que no sean vinagres, como el zumo de limón.
El proceso es siempre el mismo. Primero se echa el huevo y por encima el aceite. El orden es muy importante para que no se corte. También es importante que el huevo esté a la misma temperatura que el aceite, no de la nevera. Introducimos el brazo de la batidora hasta el fondo y comenzamos a batir. En ese momento se empieza a formar una emulsión, la mezcla estable del huevo y el aceite. Sin dejar de batir añadimos vinagre y sal al gusto.
Decimos que la mayonesa se corta cuando no se forma bien la emulsión. En lugar de espesarse, la mezcla parece que se vuelve más líquida, y por mucho que se insista con la batidora, parece que no hay marcha atrás. La razón por la que esto a veces sucede y a veces no está en la naturaleza química de las emulsiones.
Las emulsiones son mezclas entre sustancias que por su naturaleza química no se podrían mezclar. Esto sucede por ejemplo con el agua y el aceite, que no se mezclan. Cuando ponemos en contacto agua y aceite, una sustancia rehúye de la otra. Los químicos tenemos un dicho para esto: “lo semejante disuelve a lo semejante”. Con ello nos referimos a las sustancias polares y apolares.
La polaridad es una propiedad química que se caracteriza por la presencia de una marcada distribución heterogénea de las densidades electrónicas en una molécula. Cada elemento químico tiene una tendencia diferente por retener la nube electrónica de los elementos con los que enlaza cuando forma moléculas. Debido a esta desigual distribución electrónica surge la polaridad. En las moléculas en las que ocurre esto hay regiones cargadas negativamente (δ-) y otras cargadas positivamente (δ+), generando lo que llamamos momento dipolar.
El agua es una molécula polar que es útil para ilustrar esta propiedad. El agua está formada por dos hidrógenos que se unen a un oxígeno por sendos enlaces covalentes. Como el oxígeno es más electronegativo que el hidrógeno tiende a atraer más los electrones que comparten. Esto se traduce en que el oxígeno tiene más densidad de carga negativa (rojo), mientras que el hidrógeno tiene más densidad de carga positiva (azul).
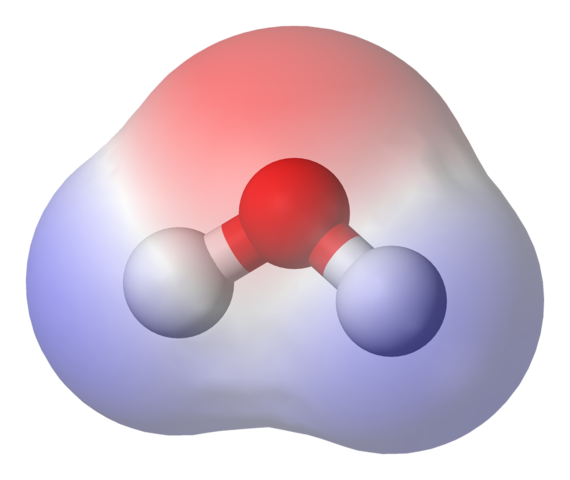
El agua es una sustancia polar. En cambio, el aceite es apolar, no presenta una distribución tan desigual de las cargas. Por este motivo el agua y el aceite no se mezclan, se repelen. Las moléculas de agua tratan de mantenerse unidas entre sí porque son afines por ser polares, y las de aceite hacen lo mismo, rehúyen de las de agua para mantenerse unidas entre sí. Como el agua es más densa que el aceite, es decir, la misma cantidad de volumen tiene más masa que el aceite, se mantendrá en el fondo, mientras que el aceite permanecerá flotando.
Sin embargo, hay muchas salsas como la mayonesa, en las que hay una mezcla estable de fase acuosa y fase grasa. Lo que en principio es imposible se vuelve posible gracias a la formación de una emulsión.
La base de la mayonesa es el aceite y el huevo. El aceite es una grasa vegetal apolar, y el huevo es esencialmente polar, ya que contiene un 80% de agua. El resto del huevo está formado por proteínas y grasa, así que el propio huevo ya es en sí mismo una emulsión, especialmente la yema, que tiene una cantidad de grasa mayor.
La razón por la que el huevo se mezcla con el aceite reside en la yema de huevo, ahí es donde encontramos la lecitina. La lecitina es un término genérico que se utiliza para designar a un tipo de grasas que son consideradas emulsionantes.
Los emulsionantes son sustancias que presentan dos extremos: uno polar y otro apolar. Así, cuando el emulsionante se distribuye entre dos fases, como agua y aceite, empieza a rodear a las gotas de aceite que se han dispersado en el agua. El extremo del emulsionante apolar, como es afín al aceite, se sitúa dentro de la gota. Mientras que el extremo afín al agua se sitúa en la parte exterior de la gota. Cuando dos gotas se acercan, el emulsionante impide que las gotas se unan entre sí. Se ha empezado a formar la emulsión.
Para hacer mayonesa es importante empezar batiendo el huevo en el fondo. De esa manera conseguimos liberar el emulsionante. A continuación, o ya sobre el huevo, tenemos el aceite que, por agitación se irá dispersando en pequeñas gotas dentro de la fase acuosa del huevo. El emulsionante irá rodeando estas gotas hasta dejarlas suspendidas en la fase acuosa.
Es importante que primero se disgregue el huevo y no al revés. Si lo hiciésemos al revés conseguiríamos el resultado inverso. El agua se iría dividiendo en gotas pequeñas, que quedarían rodeadas por el emulsionante. El extremo afín al agua del emulsionante se dirigiría hacia el centro de la gota, y la parte afín al aceite se dirigiría hacia el exterior de la gota, manteniendo a esas gotas de agua dispersas en el medio aceitoso. Esto es lo que ocurre cuando decimos que la mayonesa se corta, que hemos hecho la emulsión justo al revés.
Que la emulsión suceda en un sentido o en otro también depende de la temperatura del huevo. Al batir el huevo este se dispersa y se separa la lecitina del resto del agua. Eso se consigue gracias a la energía que aplicamos al batirlo. Si el huevo está frío necesitaremos aplicar más energía para que esto suceda, así que el resultado puede ser que el huevo no llegue a disgregarse todo lo necesario como para que el emulsionante se disponga alrededor de las gotas de aceite. Por esta razón se aconseja que el aceite y el huevo estén a la misma temperatura.
El siguiente ingrediente que se añade a la emulsión es un ácido. O bien el vinagre, que es una sustancia ácida por su contenido en ácido acético; o bien zumo de limón, que es ácido por su contenido en ácido cítrico. La función de los ácidos es estabilizar la emulsión. Las gotas de aceite rodeadas de emulsionante y dispersas en agua son más estables cuando el medio es ácido, ya que el medio ácido fomenta la repulsión entre los extremos polares y apolares. Impedir la unión entre gotas por medio de un ácido hace que la emulsión sea más estable.
Añadimos sal al gusto y listo, ya tenemos preparada la mayonesa.
-
¿Qué relación tiene esto con la cosmética?
La mayor parte de las cremas son emulsiones, presentan una fase acuosa y una fase grasa.
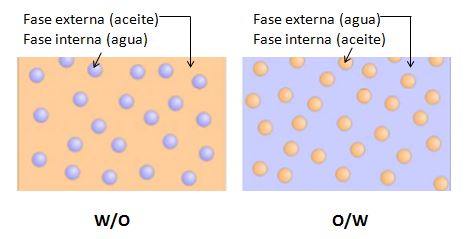
Dependiendo del tipo de cosmético que se quiera formular podemos fabricar la emulsión en un sentido u en otro: con la fase interna acuosa y la externa grasa, o al revés. Para ello empleamos emulsionantes.
Así tenemos cosméticos “oil in water” (aceite en agua), también denominados O/W. Y cosméticos “water in oil” (agua en aceite), también denominados W/O.
El 80% de los cosméticos del mercado son O/W, ya que son más frescos, ligeros y se absorben mejor. Los W/O son cosméticos más untosos. Generalmente los cosméticos para el rostro con fórmulas ligeras son O/W. Mientras que los cosméticos más viscosos diseñados para las zonas más secas del cuerpo, suelen ser W/O.
La química de la emulsión de los cosméticos O/W es como la que sucede en la mayonesa. Mientras que la química que la emulsión de los cosméticos W/O es como la que sucede cuando se nos corta la mayonesa. Lo que en cocina es un error, resulta de gran utilidad en cosmética.
Sobre la autora: Déborah García Bello es química y divulgadora científica
Carynel Guzmán
Me encantó. Gracias por esa explicación tan entendible. Saludos desde Venezuela
Luciano
No hay que olvidar que el tamaño de la partícula de emulsión cambia junto con el pH de la mezcla, lo cual indica que la cantidad de vinagre o limón juega un papel importante. La máxima estabilidad de una emulsión suele estar cerca del pH 7 (neutro). Acidificar la mayonesa a un nivel similar al del punto isoeléctrico de la parte proteica no es buena idea.
Por otra parte el añadido de sal aumenta el tamaño de la partícula a la vez que aumenta la solubilidad total. El problema es que cuando se alcanza un punto de saturación, la sal gracias a su gran poder de solvatación, secuestra la parte acuosa, separándose la parte grasa, por lo que se produce una verdadera floculación. Por lo tanto agregar demasiada sal tampoco es buena idea.
Tampoco es buena idea batir con demasiada energía. Una mayonesa bien hecha puede cortarse si seguimos batiendo innecesariamente (y es peor si se hace con batidores eléctricos). La agitación puede romper la emulsión y pasar de O/W a W/O si no tenemos cuidado.
En fin, que un poco es como decían nuestras abuelas, que de mirarla feo ya se corta una mayonesa, saludos.
Juan Antonio
A título de curiosidad: «Física y química de una salsa bearnesa fallida». Investigación y Ciencia, nº41, 1980; sección ‘Taller y laboratorio’
Lo leí cuando salió…snif…juventud, divino tesoro.
enlace en
https://www.investigacionyciencia.es/revistas/investigacion-y-ciencia/neandertales-41/fsica-y-qumica-de-una-salsa-bearnesa-fallida-4693
Juan Antonio.
Nola eta zergatik egiten da maionesa? – Zientzia Kaiera
[…] aldiz aztertu EHUko Kultura Zientifikoko Katedraren blogetan. Hain zuzen ere, sarean dago irakurgai Déborah García Bello zientzia-dibulgatzailearen ekarpena eta, benetan, irakurtzea merezi du. Hemen beste modu batera emango dira azalpenak, modu osagarrian. […]
Los motivos por los que el agua y el aceite se llevan tan mal – Periérgeia
[…] Bello DG (2019). Por qué se corta la mayonesa y qué relación tiene esto con la cosmética. Cuaderno de Cultura Científica [online] 17 de octubre. Disponible en: https://culturacientifica.com/2019/10/17/por-que-se-corta-la-mayonesa-y-que-relacion-tiene-esto-con-…; […]
The reasons why water and oil are doomed to stay separated – Periérgeia
[…] Bello DG (2019). Por qué se corta la mayonesa y qué relación tiene esto con la cosmética. Cuaderno de Cultura Científica [online] October 17. Available in: https://culturacientifica.com/2019/10/17/por-que-se-corta-la-mayonesa-y-que-relacion-tiene-esto-con-…; […]