Nanopartículas reparadoras, una estrategia para hacer frente al alzhéimer
Cada año se detectan más de 10 millones de nuevos casos de alzhéimer y hoy en día no existe ningún tratamiento efectivo contra dicha enfermedad. En octubre de este año, se ha presentado un tratamiento experimental contra el alzhéimer en un artículo publicado en la famosa revista Signal Transduction and Targeted Therapy. Dicha terapia está basada en las nanopartículas A40-POs, y supone un cambio de paradigma.
La enfermedad de Alzheimer es el tipo de demencia más común, y, desde el punto de vista molecular, se observa una acumulación excesiva de la proteína β-amiloide. La proteína amiloide hereditaria (PAA) está presente en la membrana de las neuronas, y ciertas enzimas presentes en dicho entorno (la β-secretasa en primer lugar, y la γ-secretasa en segundo) procesan la proteína, creando un fragmento de proteína o péptido denominado β-amiloide, conformado por 40 o 42 aminoácidos. La β-amiloide no es muy soluble, y se acumula en el espacio extracelular formando estructuras similares a placas fibrilares. Cuando dichas fibras se unen a las neuronas, provocan muerte celular, y así es como la enfermedad desgasta el cerebro.
Se han realizado diversos ensayos para evitar el mencionado proceso bioquímico, sea a partir de la recuperación de las células de la glía encargadas de lavar el entorno extracelular o sea buscando la inhibición de las enzimas que producen β-amiloide. En este caso, sin embargo, el equipo investigador del Instituto de Bioingeniería de Cataluña (IBEC) y del Hospital West China de la Universidad de Sichuan (WCHSU) ha tratado de reenfocar la forma de procesar la proteína β-amiloide.
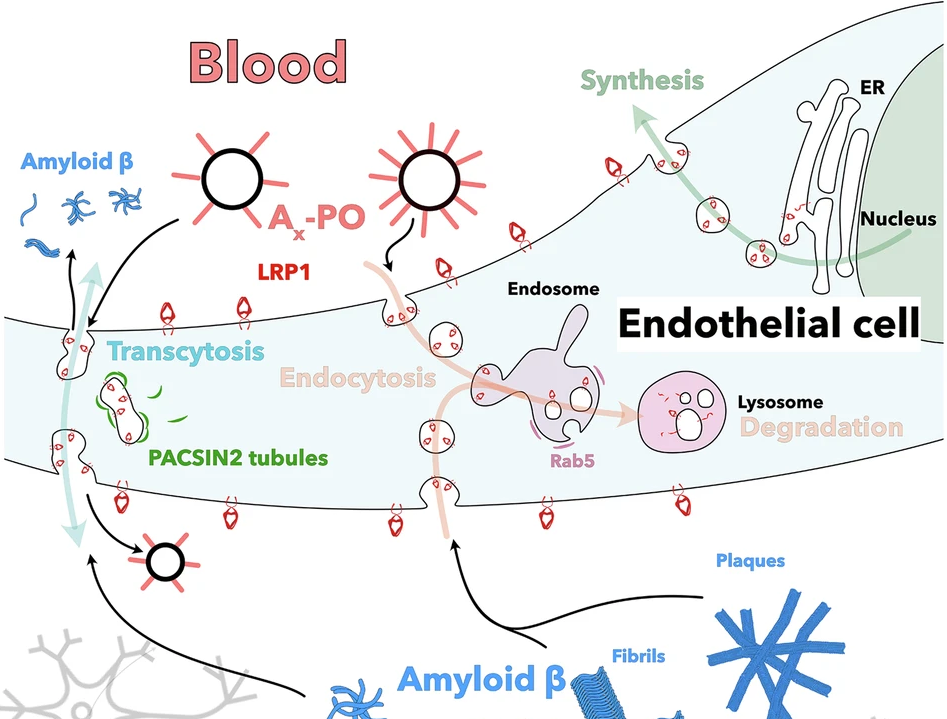
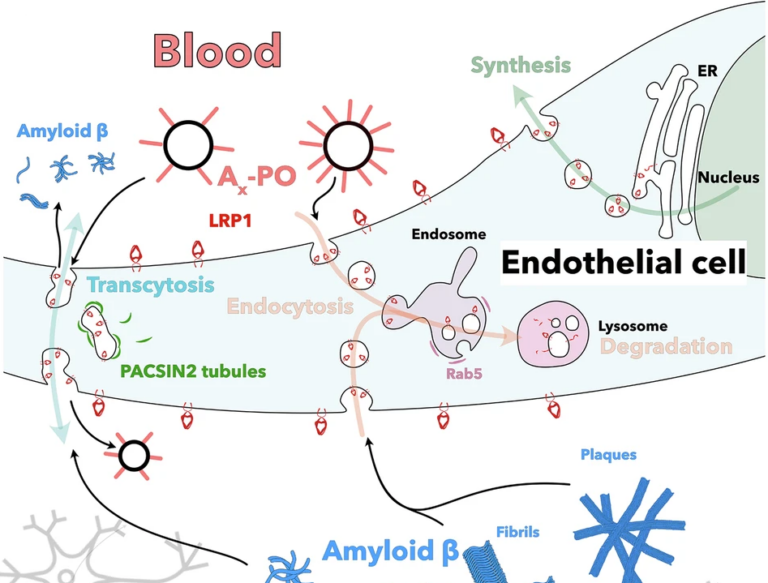
El cerebro es un órgano muy sensible, y está protegido por la barrera hematoencefálica, que es la encargada de regular la interfaz entre la sangre y el cerebro. Se encuentra formada por las células endoteliales que conforman los vasos sanguíneos, así como por los astrocitos que se encuentran situados sobre ellos. Las células endoteliales de los vasos sanguíneos del cerebro se encuentran firmemente sujetas las unas con las otras, y, encima de ellas, se encuentras los astrocitos, cerrando todavía de manera más firme dichos enlaces. Es por ello por lo que solo unas pocas moléculas que transitan por la sangre llegan a las células del cerebro. Dicho traslado selectivo no discurre solamente de la sangre al espacio celular, ya que también ocurre del espacio celular del cerebro a la sangre, de manera que los desechos que se crean en el espacio extracelular en el cerebro se expulsan a la sangre a través de unos receptores que se encuentran en las células endoteliales. Por lo tanto, la célula endotelial es la encargada de regular la interfaz entre la sangre y el cerebro.
En el caso de la enfermedad de Alzheimer, se ha observado que dicha barrera se encuentra dañada y las células endoteliales no son capaces de trasladar las placas fibrilares de β-amiloide del cerebro a la sangre, para después poder expulsarlas. Las células endoteliales sanas cuentan con un receptor llamado LRP1 en su membrana exterior, que recoge las fibras de β-amiloide y las transporta a la sangre. En el caso de esta enfermedad, las células endoteliales de la barrera hematoencefálica están dañadas, y no cuentan con receptores LPR1. Los mencionados equipos de investigación chinos y catalanes han desarrollado una nanopartícula llamada A40-POs. Dicha nanopartícula llega hasta las células endoteliales de la barrera hematoencefálica, y renueva la expresión del receptor LRP1, por lo que las células endoteliales son capaces a través de los nuevos receptores LRP1 de captar las fibras de β-amiloide del cerebro y transportarlas a la sangre, para que luego puedan ser expulsadas del cuerpo. Los ensayos se han realizado en ratones que han desarrollado la enfermedad de Alzheimer, y una hora después de inyectar las nanopartículas en el cerebro, se ha conseguido eliminar el 60% de β-amiloide acumulado. Asimismo, en algunos casos, se ha conseguido eliminar la totalidad de las placas fibrilares tras un tratamiento de 6 meses de duración.
A pesar de que puede parecer una estrategia interesante y esperanzadora, deberemos analizar detalladamente si esta nueva terapia funciona de la misma manera en otras especies animales y en humanos.
Referencias:
Chen J, Xiang P, Duro-Castano A, Cai H, Guo B, Liu X, Yu Y, Lui S, Luo K, Ke B, Ruiz-Pérez L, Gong Q, Tian X, Battaglia G. (2025) Rapid amyloid-β clearance and cognitive recovery through multivalent modulation of blood-brain barrier transport Signal Transduct Target Ther. doi: 10.1038/s41392-025-02426-1
Guo X, Yue R, Cui Z, Wang S, Jia T, Li W, Zhang W, Shan L, Li C. (2025) Advances of therapeutic strategies for Alzheimer’s disease J Neurol. doi: 10.1007/s00415-025-13456-8.
Sobre el autor: Iker Badiola Etxaburu es doctor en biología, Profesor Pleno en la Facultad de Medicina y Enfermería de la EHU, y director de la Cátedra de Cultura Científica de la EHU