Descubren los mecanismos fisiológicos que te quitan el apetito cuando estás enfermo

La situación es tan frecuente que todos la hemos vivido en algún momento de nuestra vida. Te encuentras enfermo y, acto seguido, no tienes ganas de comer nada. No importa el manjar que tengas delante, no importa que sepas que debes alimentarte bien… no hay nada que te convenza, tu estómago se cierra, tu cerebro se rebela ante el plato y, simplemente, ya no te apetece comer. ¿Por qué ocurre esto? ¿Cómo consigue el intestino comunicarse con los centros del sistema nervioso que controlan el apetito? Un estudio, publicado recientemente en Nature, ha logrado descubrir las «sorprendentes y elegantes» conexiones implicadas en este proceso fisiológico.
El trabajo lo han realizado investigadores de la Universidad de California, San Francisco (UCSF) que buscaban responder a una doble cuestión: en primer lugar, estudiar cómo el sistema inmunitario combate a los parásitos estomacales y, en segundo lugar, cómo es capaz de comunicarse y activar el sistema nervioso para modificar nuestro comportamiento. Al frente del equipo de científicos encontramos al doctor David Julius, director del Departamento de Fisiología en esta Universidad y ganador del Premio Nobel de Medicina en 2021 por desvelar otra intrigante conexión, en aquel caso entre los receptores de temperatura y el tacto.
Nuestro intestino es el hogar de millones de células especializadas que actúan como centinelas, entre ellas destacan dos tipos que hasta ahora se solían estudiar por separado:
Las células tuft, células en penacho o células del penacho intestinal, aunque se encuentran en muchos otros lugares. Son pequeñas células sensoras capaces de detectar la presencia de parásitos —gusanos intestinales y protozoos— mediante las señales químicas que estos liberan. Cuando las detectan, liberan diferentes moléculas mediadoras que activan el sistema inmunológico para combartirlas. Es importante apuntar que estas células tuft no son demasiado abundantes en comparación con el número de células presentes en nuestro intestino sin embargo, cuando aparece una amenaza (una infección, un parásito, etc.) se multiplican y proliferan rápidamente.
Por otro lado, tenemos a las células enterocromafines (EC). Su especialidad es liberar serotonina —sí, el mismo neurotransmisor relacionado con el estado de ánimo— que activa las fibras nerviosas del intestino y envía señales al cerebro relacionadas con el dolor o el malestar estomacal.
Hasta ahora no habíamos determinado claramente si estos dos tipos de células se comunicaban entre sí y es aquí donde llega este nuevo estudio demostrando que no solo lo hacen, sino que forman un sistema eficaz y elegante de comunicación en cadena desde nuestras tripas hasta el cerebro.
Para descubrir esta comunicación los investigadores modificaron genéticamente células sensoras y la colocaron en una placa junto a las células en penacho para poder estudiarlas bajo microscopio. El siguiente paso fue añadir una amenaza para ver su comportamiento, en este caso exponer las células en penacho al succinato, un compuesto que suelen liberar algunos gusanos parásitos. Cuando las células en penacho detectaron el succinato se activaron liberando acetilcolina, un neurotransmisor que funciona como molécula de señalización y que se asocia normalmente a células nerviosas, como las neuronas.
Ahora tocaba saber cómo se comportarían las células enterocromafines ante la presencia de ese neutransmisor así que, explicado de manera sencilla, recogieron las moléculas de acetilcolina que las células penacho habían liberado y las introdujeron en tejido intestinal cultivado en laboratorio que contenía células EC… y éstas respondieron liberando serotonina lo que activó las fibras del nervio vago, que transmiten señales del intestino al cerebro.
«Lo que descubrimos es que las células en penacho hacen algo que hacen las neuronas, pero mediante un mecanismo completamente diferente», explica en Science Daily, la doctora Kouki Tohara coautora principal del estudio. «Utilizan acetilcolina para comunicarse, pero sin la maquinaria celular habitual de la que dependen las neuronas para liberarla».
Señales en dos etapas
Gracias a estos experimentos los investigadores también descubrieron que las células en penacho liberan acetilcolina en dos fases distintas, lo que explica por qué la pérdida de la pérdida de apetito no suele aparecer inmediatamente después de la infección sino algo más tarde. Es lógico: inicialmente las células en penacho son pocas y liberan poca acetilcolina pero, a medida que se intensifica la respuesta inmunitaria, el número de células en penacho aumenta y se produce una liberación mayor de esa señal. Es esta segunda liberación prolongada de neurotransmisores la que se convierte en una señal suficientemente fuerte como para activar las células EC y enviar señales al cerebro. «Esto explica por qué al principio te sientes bien, pero luego empiezas a sentirte mal a medida que la infección se establece», explica David Julius, «El intestino básicamente espera a confirmar que la amenaza es real y persistente antes de indicarle al cerebro que cambie tu comportamiento».
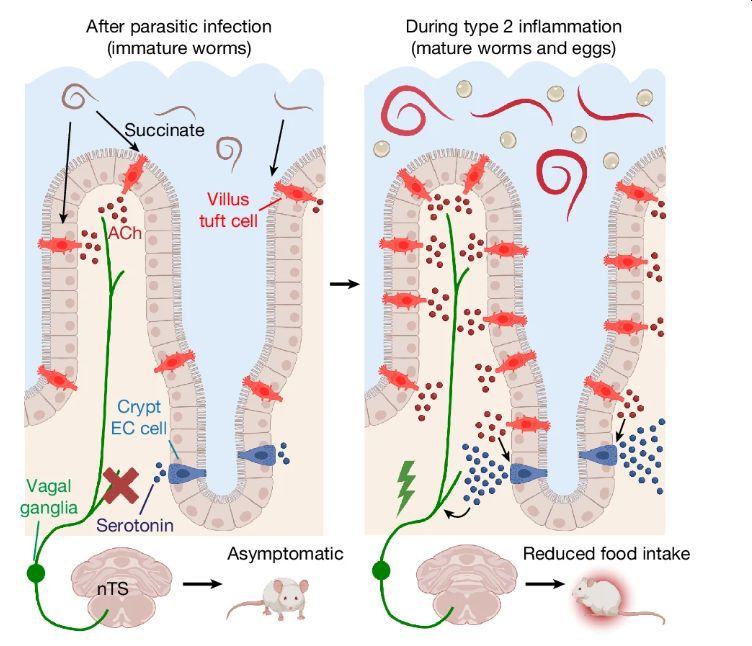
Era el momento perfecto para dar el salto desde los primeros experimentos in vitro bajo microscopio hasta la confirmación con modelos animales. Para ello estudiaron ratones infectados con gusanos parásitos y un grupo de control con ratones a los que se modificó para que no pudieran producir acetilcolina en sus células penacho. Los resultados confirmaron esta comunicación ya que los ratones con función normal de las células penacho comían menos a medida que avanzaba la infección mientras que los que no podían producir ese neutransmisor seguían comiendo con normalidad. «Esto confirmó que la vía de señalización influye directamente en los cambios de apetito».
El estudio no solo arroja luz a la cuestión de por qué no tenemos ganas de comer cuando estamos enfermos sino que también abre la ventana a aplicaciones más prácticas como «el desarrollo de nuevos tratamientos para los síntomas relacionados con las infecciones parasitarias». Conocer el circuito célula tuft → acetilcolina → célula enterocromafine → serotonina → nervio vago → cerebro— permite identificar puntos concretos donde se podría intervenir farmacológicamente para aliviar síntomas como la anorexia asociada a infecciones, la hipersensibilidad visceral o las náuseas crónicas.
Además, las células en penacho se encuentran en diversas partes del cuerpo, incluyendo las vías respiratorias, la vesícula biliar y el sistema reproductivo, no solo en el intestino. Las alteraciones en esta vía de señalización recientemente identificada podrían influir en afecciones como el síndrome del intestino irritable, las intolerancias alimentarias y el dolor visceral crónico.
Para finalizar, es conveniente recordar que en ciencia lo normal es que cuando se consigue algún descubrimiento también aparecen nuevas preguntas. El misterio de cómo las células tuft liberan acetilcolina sin tener el aparato molecular habitual para ello sigue abierto, y resolverlo podría revelar mecanismos biológicos completamente nuevos con aplicaciones más allá del intestino, en órganos como los pulmones o la vesícula biliar, donde también existen este tipo de células.
Referencias científicas y más información:
University of California, San Francisco (2026) Scientists discover why your appetite suddenly disappears when you’re sick ScienceDaily
Touhara, K.K., Xu, J., Castro, J. et al. (2026) Parasites trigger epithelial cell crosstalk to drive gut–brain signalling Nature doi: 10.1038/s41586-026-10281-5
Sobre el autor: Javier Peláez (@Irreductible), es escritor y comunicador científico. Autor de «500 Años de Frío» (2019) y «Planeta Océano» (2022), también es guionista en el programa de TVE «Órbita Laika» y ganador de tres premios Bitácoras, un premio Prisma a la mejor web de divulgación científica y un Premio Ondas al mejor programa de radio digital.
