En los límites del frío
Cuando uno emprende un proyecto en biotecnología tiene que tener claro que modificación quiere hacer y con qué finalidad. Por ejemplo: hacer plantas que sean resistentes a condiciones adversas (técnicamente estrés) ¿Cómo hacemos una planta resistente a plagas? Pues para eso hace falta conocer la plaga. Puede ser que en la naturaleza esa plaga sea sensible a una proteína, o que la plaga sea un virus que utiliza una proteína de la planta para infectar. Si haces que la planta exprese la proteína tóxica para el insecto, o que deje de expresar la proteína que utiliza el virus para infectar habrás conseguido tu objetivo. En la naturaleza son frecuentes las poblaciones resistentes determinada enfermedad por llevar alguna mutación en su genoma. Las plantas transgénicas resistentes a insectos, virus o herbicidas se basan en este principio. Expresan un gen de otro organismo que específicamente es tóxico para el insecto, degrada el herbicida o impide la infección del virus.
El problema es si a lo que queremos hacer frente es un estrés ambiental, como puede ser el frío. Para empezar aquí no tendremos una bala mágica. A medida que baja la temperatura determinados procesos biológicos empiezan a fallar. Un truco para diseñar estrategias exitosas es identificar cuáles son esos procesos, los llamados factores limitantes y hacer plantas transgénicas que sean capaces de hacer frente a esos primeros fallos, lo que aumentara el nivel de tolerancia global. Para entendernos. Imagina que vas a arrancar el coche y no funciona por qué el depósito está vacío. Si le pones gasolina, el coche va. Ahora imagina que quieres que vaya más rápido ¿le pones más gasolina? No, porque el factor limitante ya no es ese, sino la potencia del motor. Por lo tanto es importante tener claro cuáles son los procesos que se ven afectados por las condiciones adversas y en qué orden, para no diseñar plantas con motores muy potentes, pero sin gasolina, que no funcionarían bien en condiciones adversas.
Una forma de abordar este problema es utilizar levadura. En ciertos aspectos se comporta como una planta, pero además crece muy rápido y es fácil poner y quitarle genes. Para ver cuáles son los factores limitantes podemos hacer una población de células de levadura que al azar aumente la expresión de un gen determinado de la propia levadura. A esta población la ponemos a crecer a una temperatura tan fría que la levadura no puede crecer. Si por casualidad alguno de estos genes codifica algo que mejora un factor limitante, esta colonia crecerá mientras que el resto se quedará parada. Así podremos identificar que gen es y nos dará pistas sobre el factor limitante. Esto tiene interés no solo para planta, sino también para la propia levadura, puesto que aumentar la capacidad de fermentar en condiciones de frío puede ser útil para la producción de cervezas de tipo Ale o de algunos vinos que se fermentan en frío para evitar la aparición de determinados aromas.
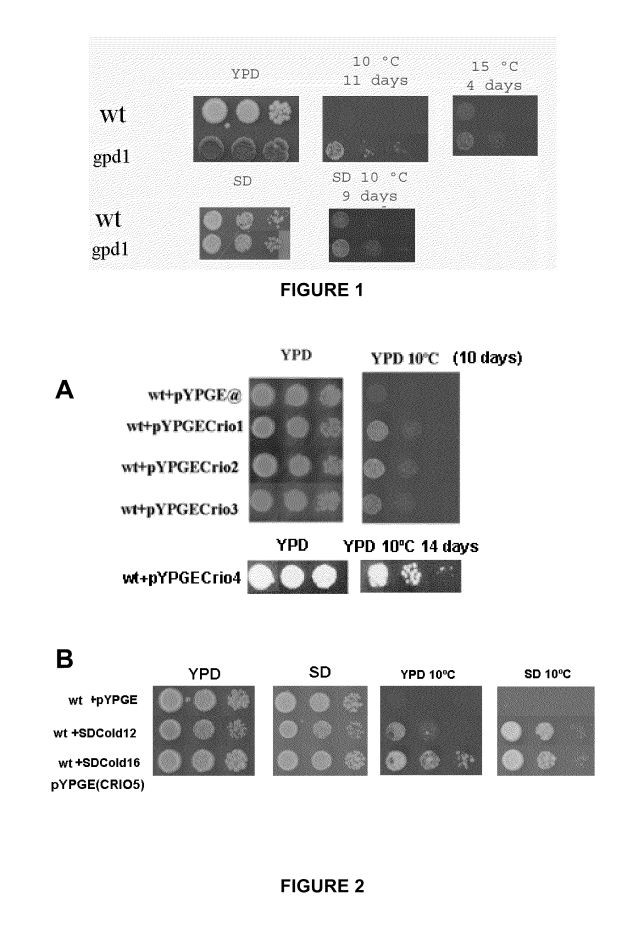
¿Qué pasa cuando haces este proyecto en levadura y la pones a crecer a 10ºC?. Pues que casi todo lo que te sale tiene que ver con el transporte de un determinado aminoácido, el triptófano, o algún gen relacionado con la biosíntesis de lípidos de membrana. Esto tiene su lógica. La levadura que se utiliza en laboratorio no puede sintetizar triptófano y lo tiene que tomar del medio. La toma de triptófano depende de dos transportadores de la membrana plasmática, que son muy sensibles a la fluidez de esta. En frío la membrana pierde fluidez, de la misma forma que el aceite solidifica. Si aumentamos esta fluidez o aumentamos el número de transportadores de triptófano, la célula aguanta mejor.
Ya tenemos identificado el depósito de gasolina. Pero ¿qué pasa si lo tenemos lleno? Podemos utilizar una cepa capaz de sintetizar triptófano o añadir un exceso de triptófano al medio de crecimiento. Entonces el triptófano dejará de ser limitante y podremos identificar la siguiente diana. Por lo tanto repetimos la misma estrategia poniendo triptófano en el medio y creciendo las levaduras a 8ºC. Todo lo que salieron eran genes relacionados con la toma de fosfato inorgánico. Ya teníamos el motor localizado. Además, la toma de fosfato no se puede solventar de forma metabólica, puesto que al ser un nutriente mineral se tiene que tomar del medio.
Entre los genes identificados encontramos uno que no estaba caracterizado como gen, es decir, algo que en el genoma de levadura estaba anotado como ORF, abreviatura en inglés de pauta abierta de lectura, un trozo de la secuencia de ADN con señal de inicio y de parada pero que nadie ha demostrado que realmente codifique un gen, por lo que tuvimos el privilegio de bautizar e indicar que aumenta la tolerancia a frío al ser sobreexpresado en levadura y que está implicado en la toma de fosfato inorgánico. Como somos poco originales le llamamos CTO1 por Cold TOlerance 1. Por lo tanto, ya sabéis, si queréis hacer cerveza Ale, añadid triptófano y fosfato en el medio y fermentará mejor.
Este post ha sido realizado por JM Mulet (@jmmulet) y es una colaboración de Naukas con la Cátedra de Cultura Científica de la UPV/EHU.
Referencia:
FEMS Yeast Res. 2015 May;15(3). pii: fov008. doi: 10.1093/femsyr/fov008. Epub 2015 Feb 26.
Uptake of inorganic phosphate is a limiting factor for Saccharomyces cerevisiae during growth at low temperatures.
Vicent I, Navarro A, Mulet JM, Sharma S, Serrano R.