Llega la segunda generación de ingredientes funcionales
El mercado de los alimentos funcionales tiene un problema. Aunque este tipo de productos factura casi 33.000 millones de dólares en todo el planeta, las pocas evidencias científicas acerca de su efectividad han despertado el escepticismo entre el consumidor. Muchas de las propiedades saludables que se han publicitado durante años no han demostrado estar sustentadas por la ciencia y, como resultado, la Autoridad Europea de Seguridad Alimentaria ha denegado miles de solicitudes de las empresas alimentarias basadas en la publicidad engañosa. Además, la sobresaturación del mercado, repleto de zumos enriquecidos en vitaminas, productos con efecto Bífidus, margarinas con esteroles, prebióticos, simbióticos, etc., ha provocado que estos productos ya no despierten la atención del consumidor como lo hacían hace unos años. Por esta razón, los departamentos de investigación y desarrollo de las empresas de alimentación buscan afanosamente nuevos ingredientes con los que enriquecer los alimentos funcionales. En este artículo les voy a mostrar, entre otras muchas cosas, cómo la ciencia les está echando una mano.

Los nuevos ingredientes funcionales deben cumplir tres premisas: que sean innovadores, que posean propiedades saludables y que sean de fácil producción. Para alcanzar este triple objetivo los investigadores están intentando mejorar la producción de nuevos metabolitos presenten en el reino vegetal para los cuales lo los procesos de síntesis química son complicados.
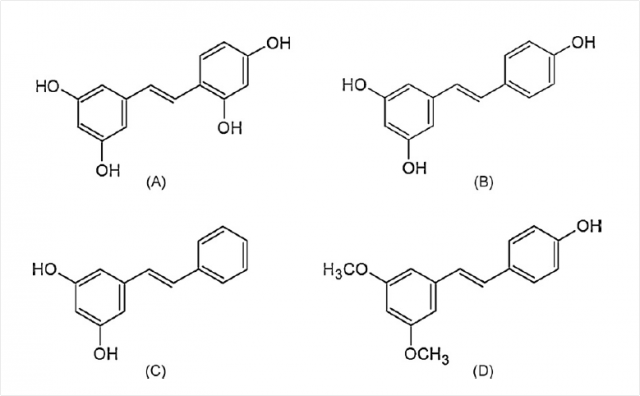
Recientes estudios muestran como moléculas pertenecientes al grupo de los estilbenos podrían cumplir, al menos, dos de las propiedades que se le piden a los nuevos ingredientes funcionales. Por una parte, se les están descubriendo numerosas propiedades saludables “in vitro” que luego habrá que comprobar si se reproducen “in vivo”. Por otra parte, pocos alimentos funcionales se han enriquecido en estilbenos, lo que los convierte en un grupo de compuestos que pueden revolucionar el mercado. Sin embargo, esta familia de hidrocarburos aromáticos de bajo peso molecular, entre los que se encuentran el oxyresveratrol, el resveratrol, el pterostilbeno o la pinosilvina, presentan dos importantes inconvenientes: no son fáciles de sintetizar y se encuentran a muy baja concentración en un grupo muy reducido de plantas.
Para solucionar estos problemas es necesario el desarrollo de estrategias que permitan incrementar la productividad de estilbenos usando cultivos in vitro. Una de esas estrategias consiste en añadir a los cultivos celulares agentes que incrementen su producción. Un ejemplo son los elicitores. ¿A qué me refiero?
La elicitación es un conjunto de técnicas en las que se somete las células a factores externos, induciendo mecanismos de defensa que en ocasiones incrementan la síntesis de metabolitos específicos. Dichos factores son llamados elicitores y se clasifican de acuerdo a su naturaleza, en bióticos (quitosano, metil jasmonato, alginato, extractos fúngicos) y abióticos (metales pesados, estrés térmico, estrés osmótico).
En el caso de la familia de compuestos protagonista de este post, los estilbenos, el elicitor que tradicionalmente mejor resultado ha dado para incrementar su producción en cultivos de células vegetales es el metil jasmonato, un compuesto orgánico volátil de la familia de los jasmonatos que actúa como regulador del crecimiento de las plantas y al que se atribuyen efectos importantes sobre el desarrollo vegetal y sobre las respuestas a diferentes tipos de estrés ambiental.
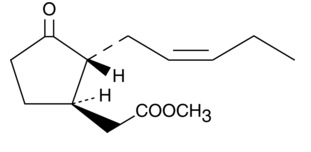
Diferentes estudios muestran como el jasmonato es capaz de aumentar ligeramente la producción de compuestos bioactivos de gran interés como es el caso del resveratrol. Sin embargo, el uso de metil jasmonato como único elicitor no es capaz de incrementar la producción de este famoso estilbeno en cantidades suficientes como para enriquecer alimentos funcionales. ¿Y cómo solucionamos este nuevo problema? Añadiendo a los cultivos celulares otras moléculas que, conjuntamente con el metil jasmonato, produzca el efecto deseado.
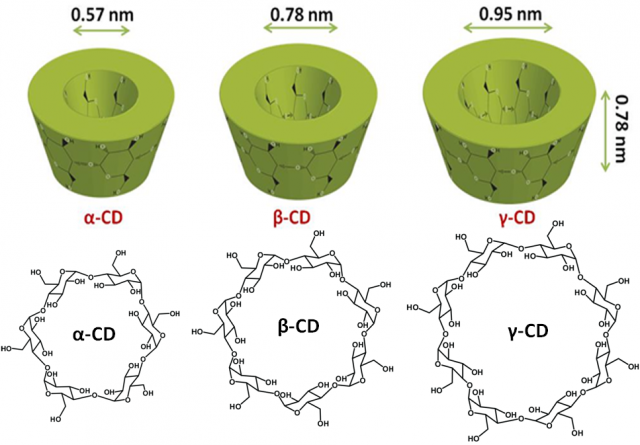
¿A qué compuestos me refiero? A las ciclodextrinas, moléculas de glucosa unidas por enlaces α-1-4-glucosídicos y que se pueden obtener de forma natural mediante la acción de enzimas microbianas. El número de unidades de glucosa determina el nombre de cada ciclodextrina, que es designada por una letra griega: α-CD (6 unidades de glucosa), β-CD (7 unidades de glucosa) γ-CD (8 unidades de glucosa), etc. Además, las ciclodextrinas están sujetas a posibles adiciones, sustituciones o eliminaciones que den lugar a modificaciones en su estructura.
Diversos autores han demostrado como la adición simultánea de ciclodextrinas y metil jasmonato a cultivos celulares dispara la producción de resveratrol hasta niveles muy significativos. Sin embargo, dichos autores no han sabido dilucidar la razón de este comportamiento. Si el objetivo final es producir mucho resveratrol para enriquecer alimentos funcionales es imprescindible conocer las bases moleculares del proceso observado. Es la única forma de mejorarlo y alcanzar nuestro objetivo.
Habitualmente se ha atribuido el fenómeno observado a un efecto sinérgico entre el metil jasmonato y las ciclodextrinas sin tener en cuenta la gran capacidad de las ciclodextrinas para encapsular, mediante la formación de complejos de inclusión, una amplia variedad de moléculas orgánicas e inorgánicas, comúnmente denominadas moléculas huésped, dentro de su cavidad interna. La encapsulación de moléculas en el interior de las ciclodextrinas tiene una serie de ventajas entre las que destacan la estabilización de sustancias sensibles a la luz y/o oxígeno, la fijación de sustancias volátiles, la protección de distintas sustancias frente a la degradación por microorganismos, el aumento de la solubilidad, absorción y biodisponibilidad de diversas moléculas o el enmascaramiento de colores, sabores y aromas desagradables.
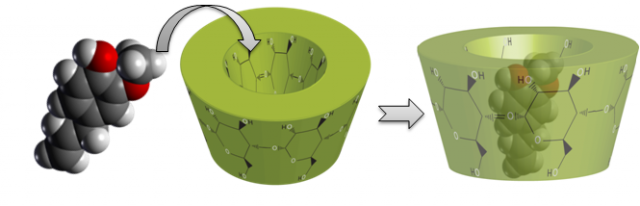
¿Y tienen capacidad las ciclodextrinas para encapsular el metil jasmonato de forma que el complejo de inclusión formado por ambos sea el causante del fuerte incremento del resveratrol en cultivos celulares? Además, en el caso de tener esa capacidad… ¿Cuál de las decenas de ciclodextrinas conocidas encapsula mejor el metil jasmonato? ¿Es necesario ir probándolas una a una en el laboratorio hasta dar con la ciclodextrina óptima?
La química computacional premiada con el Premio Nobel de Química 2013, a través del llamado cribado virtual, nos dará la respuesta a todas estas preguntas.
El cribado virtual es el uso de herramientas de modelado molecular o química computacional para cribar in-silico (por computadora o vía simulación computacional) una librería que contiene información estructural sobre gran cantidad de ligandos (incluso decenas de millones de ellos). En el caso que nos ocupa un correcto cribado nos permitirá encontrar, entre todas las ciclodextrinas componentes de dicha librería y sin necesidad de ir probándolas una por una en el laboratorio, cuál es la óptima para encapsular al metil jasmonato y así producir mucho resveratrol.
¿Qué elementos son necesarios para hacer un correcto cribado virtual? Dos principalmente. Una amplia librería donde buscar ligandos y un potente ordenador que haga las simulaciones correspondientes mediante los programas adecuados. Para poder procesar grandes librerías con millones de compuestos, los métodos de cribado virtual deben ser lo suficientemente rápidos para poder realizar el proceso en un espacio de tiempo razonable y poder además identificar “las agujas en el pajar”.
¿De qué métodos de cribado se dispone? Para realizar cribado virtual podemos usar muchas técnicas distintas. Tenemos rápidas e imprecisas (tales como farmacóforos), de mediana precisión (docking molecular), de precisión alta (dinámica molecular) y por último de muy alta precisión (métodos cuánticos).
Y de todos estos métodos… ¿cuál es el mejor para predecir la posible unión entre el metil jasmonato y las ciclodextrinas? Según hemos demostrado el grupo de investigación”Bioquímica y Biotecnología enzimática” de la Universidad de Murcia, al cual pertenezco, la técnica de docking molecular es la mejor opción para realizar el cribado. En el campo del modelado molecular este es un método que predice la conformación preferida de una molécula, al estar unida a otra, con el fin de formar un complejo estable. En las siguientes imágenes, obtenidas utilizando la base de datos Protein Data Bank (una base de datos donde se puede ver la estructura tridimensional de proteínas y ácidos nucleicos) y los programas informáticos AutoDock Vina y PyMOL, se observan representaciones tridimensionales de los complejos formados entre diferentes ciclodextrinas y el metil jasmonato. Estas imágenes han sido obtenidas a partir del docking molecular.
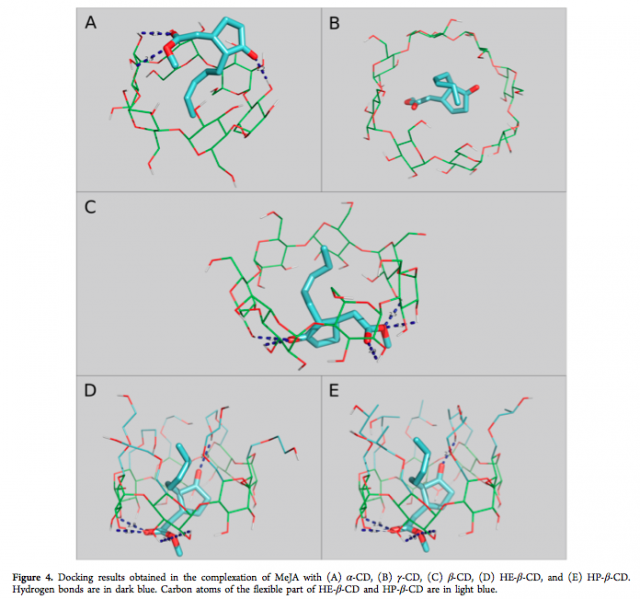
Según se puede apreciar en esas imágenes todas los tipos de ciclodextrinas empleadas son capaces de interaccionar con el metil jasmonato. Además, se puede ver el tipo de enlace entre el agente encapsulante y el ligando. ¿Y cómo sabemos cuál es la ciclodextrina óptima? El docking molecular también es capaz de predecir la fuerza de la asociación usando unas funciones de puntuación. Según nuestros estudios computacionales las dos ciclodextrinas con mejor capacidad de encapsular el jasmonato son β-CD (aquella formada por 7 anillos de glucosa) y su derivada HP-β-CD.
Si ustedes están siguiendo correctamente este post se darán cuenta que empleando la bioinformática hemos seleccionado solo dos ciclodextrinas entre centenas de existentes. Este proceso ahorra trabajo y dinero…y todo gracias a los padres de la química computacional, los Premios Nobel de Química del 2013: el austríaco Martin Karplus, el sudafricano Michael Levitt y el israelí Arieh Warshel.

¿Hemos acabado? No. Para que los resultados obtenidos mediante química computacional a través de grandes ordenadores sean definitivos deben complementarse con experimentos en los laboratorios que confirmen los resultados predichos. La química computacional y la química tradicional deben ir cogidas de la mano. En nuestro caso elegimos como técnica de análisis químico la cromatografía líquida. En la siguiente imagen se observa que, al introducir en un sistema cromatográfico concentraciones crecientes de ciclodextrinas, el tiempo de retención del metil jasmonato disminuyó conforme se aumentaba la presencia de ciclodextrinas en el medio… lo que indica experimentalmente que, tal como predijo la química computacional, las ciclodextrinas son capaces de encapsular al metil jasmonato ya que afectan a su comportamiento cromatográfico.
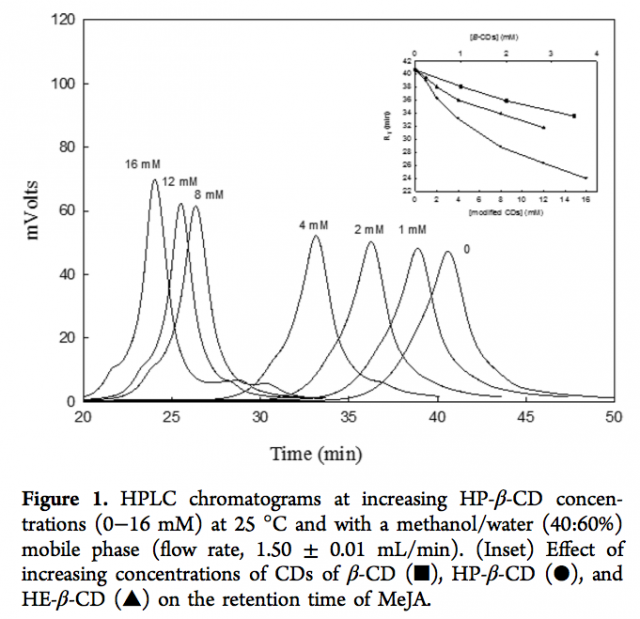
Ya tenemos la explicación al fenómeno observado por muchos científicos y que puede ser determinante para la producción de nuevos ingredientes bioactivos que refloten el mercado de los alimentos funcionales. La presencia conjunta de ciclodextrinas y metil jasmonato incrementa la producción de resveratrol gracias a la encapsulación molecular. El siguiente paso será optimizar dicha producción para, a continuación, enriquecer alimentos funcionales con este estilbeno. Por último, y para no caer en la publicidad engañosa, habrá que evaluar si las propiedades in vitro demostradas por este estilbeno se reproducen en estudios en humanos.
Estimados lectores, cuando comencé a escribir este post me propuse trasmitirles dos ideas que son fundamentales para comprender la investigación científica.
La primera de ellas es que entiendan la importancia de conocer los fenómenos moleculares que ocurren a pequeña escala para luego poder diseñar procesos a gran escala… o dicho de otro modo, la estrecha relación existente entre la investigación básica y la aplicada.
La segunda, igual de importante, es que la ciencia es absolutamente interdisciplinar. Relean este artículo y se darán cuenta que para solucionar un problema relacionado con la alimentación hemos necesitado a la fisiología vegetal, a la encapsulación molecular, a la química computacional, a la bioinformática, al análisis químico y a muchas otras ramas de la ciencia de las que no les he hablado… ¿de verdad alguien piensa que la ciencia entiende de fronteras disciplinares?
Referencia:
López-Nicolás JM, Escorial Camps M, Pérez-Sánchez H, García-Carmona F. J (2013) “Physicochemical and thermodynamic characterization of the encapsulation of methyl jasmonate by natural and modified cyclodextrins using reversed-phase high-pressure liquid chromatography”. Agric Food Chem. 27;61(47):11347-54. DOI: 10.1021/jf402920p
Este post ha sido realizado por Jose M. López Nicolás (@ScientiaJMLN) y es una colaboración de Naukas con la Cátedra de Cultura Científica de la UPV/EHU.

Hitos en la red #110 – Naukas
[…] que de homeópata no tiene nada; y este amplio informe de José Manuel López Nicolás porque Llega la segunda generación de ingredientes funcionales. También los efectos perniciosos de las cosas que sí funcionan en Experimentos que te cambian la […]
Llega la segunda generación de ingredientes funcionales | SCIENTIA
[…] Para seguir leyendo pinchen aquí. […]