¿Qué es el pH?

A menudo en cosmética se hace referencia al pH. También en productos de limpieza e higiene, y en alimentación. Incluso hay dietas anticientíficas, como la dieta alcalina, que dicen fundamentarse en el concepto de pH.
Para entender qué es el pH, primero debemos entender qué es un ácido.
A lo largo de la historia hemos dado descripciones cada vez más sofisticadas de qué es un ácido y, en consecuencia, hemos diseñado una variable para medir el nivel de acidez de una sustancia: el pH.
Al principio hablábamos de ácidos como sustancias con una serie de propiedades comunes con respecto al sabor. El sabor ácido del limón o del vinagre, por ejemplo. Ahora sabemos que estos sabores dependen del ácido cítrico y del ácido acético, respectivamente. Además, descubrimos que estas sustancias de “sabor ácido” tiñen de rojo determinados pigmentos, como el tornasol que se extrae de algunos líquenes. Tradicionalmente se extrae de roccellas y dendrographas. También atacan al mármol y reaccionan con algunos metales desprendiendo gas hidrógeno. El químico Robert Boyle fue el primero en llamar ácidos a estas sustancias con propiedades similares. Fue en 1663.
Hay sustancias que son opuestas a los ácidos. Que en contacto con los ácidos amortiguan sus propiedades. Son sustancias de sabor amargo, que producen sensación jabonosa en la piel y tiñen de azul el tornasol. A estas sustancias las denominamos álcalis, del árabe al kali, que significa cenizas vegetales.
Cuando mezclamos una sustancia ácida con otra alcalina se obtiene una sal que pierde las propiedades de ambas. Así los álcalis recibieron más tarde el nombre de bases, del griego basis, que significa fundamento para la obtención de sales. Cuando se mezcla un ácido con una base se forma una sal.
Sabemos que las propiedades de cualquier sustancia dependen de su composición y de su estructura. El químico Lavoisier conjeturó que los ácidos eran sustancias que contenían un elemento químico que en 1777 denominó oxígeno. La palabra oxígeno está formada por dos raíces griegas, oxys, ácido, por el sabor punzante de estas sustancias, y genes, productor o engendrador. De modo que la palabra oxígeno significa engendrador de ácidos.
Sin embargo, años más tarde se descubrieron otras sustancias con propiedades ácidas que no contenían oxígeno en su composición. Como el ácido muriático (hoy llamado ácido clorhídrico, HCl) que sirvió al químico Humphry Davy para conjeturar en 1810 que la acidez de las sustancias depende del hidrógeno, no del oxígeno.
Más adelante, el químico Justus von Liebig quiso completar la idea de Davy. En 1838 propuso la existencia de dos tipos de hidrógeno, siendo el hidrógeno que puede sustituirse por metales el responsable de las propiedades de los ácidos.
El químico Svante August Arrhenius fue más allá. En 1887 propuso que el hidrógeno ácido era hidrógeno que se desprendía de las sustancias ácidas como ion hidrógeno, escrito H+ y coloquialmente denominado protón.
Esto permitió dar una definición más concreta sobre las bases. Arrhenius conjeturó que, si las bases neutralizaban a los ácidos sería porque contienen un ion de carga opuesta que da lugar a la formación de una sustancia que no es ni ácida ni básica, sino neutra. Pensó que ese ion sería el OH–, ya que al unirse al H+ de los ácidos, daría lugar a la formación de agua, H2O.
Las definiciones de Arrhenius para los ácidos y las bases son limitadas, sobre todo para las bases, ya que no todas las sustancias de propiedades básicas contienen OH–, como por ejemplo una conocida base que utilizamos como producto de limpieza: el amoníaco, NH3. Sin embargo, y a pesar de sus inconvenientes, esta teoría estuvo vigente casi cuarenta años, durante los cuales se fueron sucediendo nuevas ideas que darían lugar a teorías más completas.
El químico Johannes Nicolaus Brønsted y el químico Thomas Martin Lowry, simultáneamente, pero siguiendo líneas de trabajo diferentes, propusieron en 1923 una definición más precisa sobre los ácidos y las bases. Esta definición forma parte de la que conocemos como teoría ácido-base de Brönsted-Lowry. Según esta teoría, los ácidos son sustancias capaces de donar un protón (H+), mientras que las bases son capaces de aceptarlos. De esta manera las reacciones entre ácidos y bases pueden interpretarse como reacciones de transferencia de protones. Así por ejemplo el amoníaco (NH3), es una base porque es capaz de captar H+ y formar el ion amonio (NH4+).

En la actualidad existen teorías más completas que la de Brönsted-Lowry, siendo la más conocida la teoría de Lewis de 1938, que se basa en un concepto electrónico de mayor complejidad. Aun así, la definición de uso más común de ácidos y bases es la que formularon Brönsted y Lowry.
A partir de la definición de ácido de Brönsted y Lowry, el químico Søren Peter Lauritz Sørensen introdujo por primera vez en 1909 el concepto de pH. El pH está ligado a la cantidad de H+.
Mediante el uso de electrodos podemos medir la cantidad de H+ presente en una disolución, es decir, la concentración de H+.
Para darle una numeración más manejable, Sørensen decidió aplicar la función logaritmo sobre el valor de la concentración de H+. Esa es la definición matemática del pH: el logaritmo en base 10, cambiado de signo, de la concentración de H+, cuando ésta se expresa en moles por decímetro cúbico.
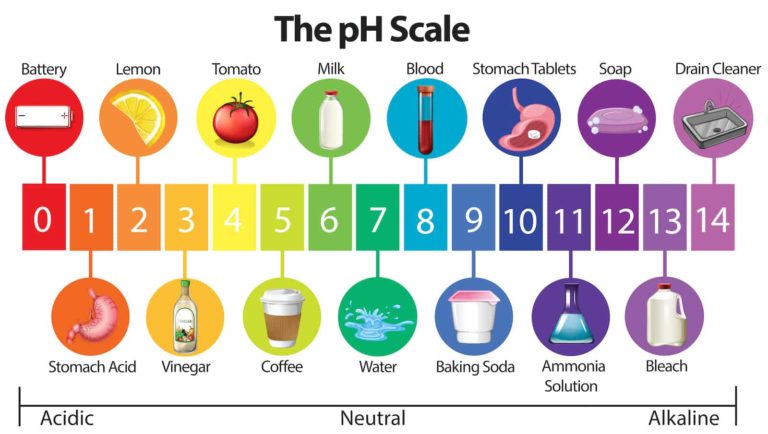
De esa manera obtuvo una escala de pH, que es la que utilizamos en la actualidad, que normalmente oscila entre los valores 0 y 14. Así, el valor de pH 7 se corresponde con las sustancias neutras. El agua pura tiene pH 7. Las sustancias ácidas son las que tienen un pH inferior a 7, y las básicas superior a 7.
En la actualidad, para medir el pH utilizamos un electrodo sensible a los H+. Se conoce como pH-metro (pronunciado peachímetro). Cada vez que se usa hay que calibrarlo usando unas disoluciones de referencia cuyo pH es conocido y sirven de patrón para que el aparato construya la escala de pH.
Hay otras maneras de medir el pH. Una manera no tan precisa, pero útil, es el uso de indicadores colorimétricos de pH. Según el color que adquieren, podemos saber el valor aproximado del pH. El más antiguo y que se sigue usando es el tornasol. En disoluciones ácidas, de pH inferior a 5, el tornasol es rojo, mientras que cuando el pH excede de 8 se vuelve azul.
Los indicadores son ácidos débiles, es decir, aunque tengan preferencia por donar iones H+, también coexisten con otra forma básica que puede aceptarlos, y cada una de estas formas presenta una coloración diferente.
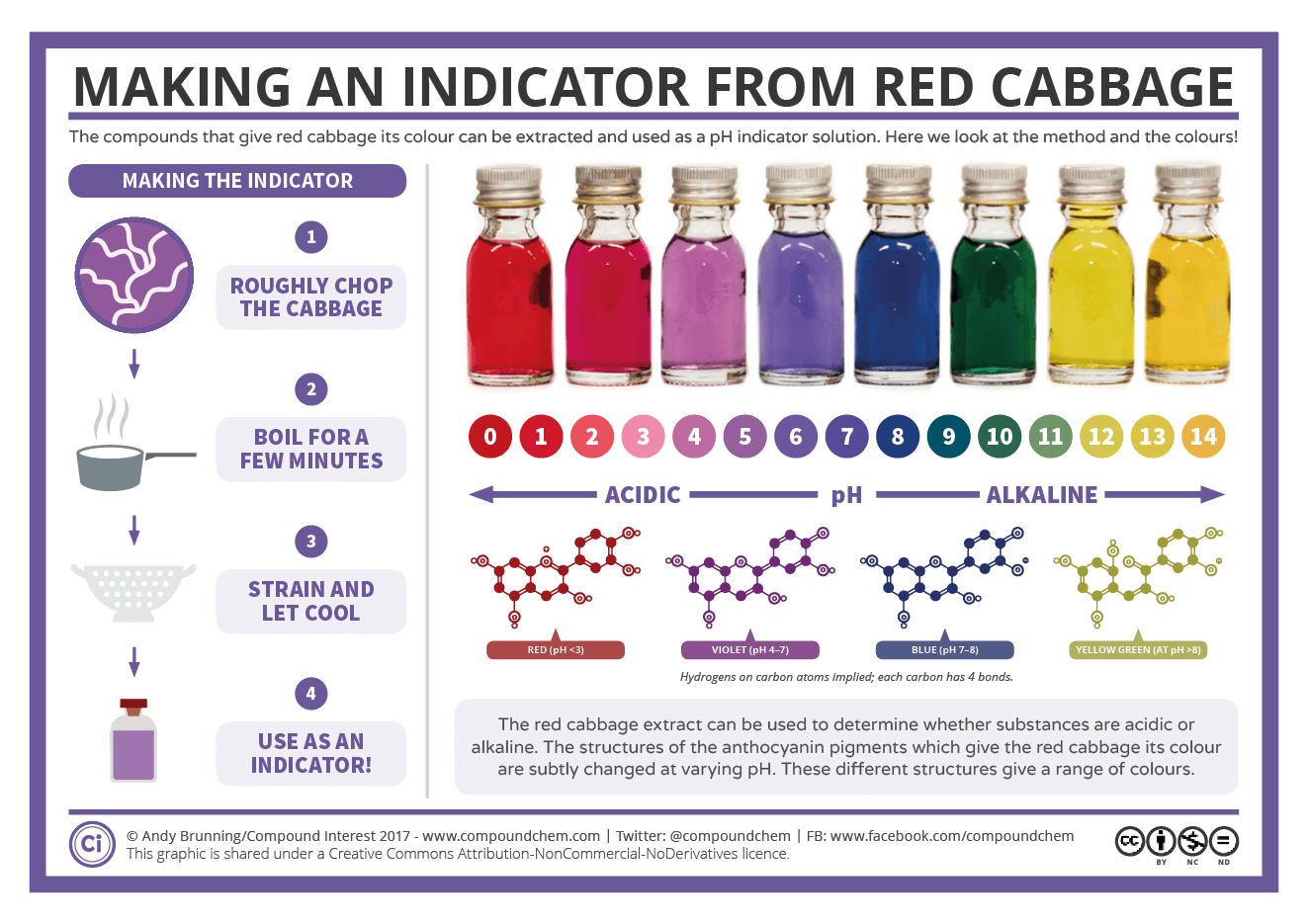
Otro indicador colorimétrico de origen vegetal son las antocianinas. Las antocianinas de la col lombarda se pueden aprovechar para fabricar un papel indicador ácido-base casero. Para eso se empapa un papel de filtro con zumo concentrado de lombarda macerada y hervida. El papel se deja secar y finalmente se corta en tiras para obtener varios indicadores de pH. A pH entre 1 y 2 el color del zumo de lombarda será rojizo, a pH 4 será color ciruela, a pH 5 será púrpura, a pH 6-7 será azul, a pH 8 será azul verdoso, a pH 9-10 será verde esmeralda, a pH 10-11 será verde hierba, a pH 12-13 será verde lima y a pH 14 amarillo.
En el laboratorio utilizamos varios indicadores de pH. Los más habituales son la fenolftaleína, el naranja de metilo o el azul de metileno.
El pH es una variable química que nos permite medir el grado de acidez de una sustancia. Su definición tiene cierta complejidad, y aun así ha calado en el lenguaje coloquial. Sin embargo, la palabra pH no siempre se emplea de manera correcta. De hecho, ignorar el significado del pH, igual que ignorar qué es un ácido o qué es un álcali, hace que las decisiones también sean ignorantes. Como decantarse por la compra de un producto, sin entender si su pH lo hace mejor o peor, o decidir seguir una dieta aberrante porque presuntamente está basada en este concepto científico. Por cierto, el zumo limón no es alcalino, es ácido.
Sobre la autora: Déborah García Bello es química y divulgadora científica
Carynel Guzmán
Excelente publicación! Me encantó
Rawandi
Muy buen artículo. Se me ocurre otro ejemplo de confusión generada por el desconocimiento de la escala de pH. Con frecuencia, los medios hablan de la acidificación del océano debido al aumento de dióxido de carbono, y el público tiende a suponer que el océano ya es ácido, cuando en realidad es alcalino (pH 8) y simplemente se está haciendo menos alcalino.
Vidas salvadas por la cloración del agua — Cuaderno de Cultura Científica
[…] Si se añade cloro gas (Cl2), el cloro reacciona con el agua formando diferentes especies según el pH del agua: perclorato, hipoclorito, ácido clorhídrico, ácido hipocloroso… También pueden utilizarse […]
Sørensen, el inventor del pH – Historia F+Q
[…] https://culturacientifica.com/2019/11/28/que-es-el-ph/ […]
Cloro y coronavirus, una relación complicada para las piscinas – Cool Pool
[…] mediciones diariamente. Lo niveles correctos de pH deben encontrarse entre 7,2 y 7,6. Cuando el pH está debajo de estos niveles quiere decir que el agua tiene una acidez que perjudica el agua y […]
Mariana trai ni
Muy claro y completo el articulo.
Aclarado de Piel con Técnica de Peeling – ELAESI
[…] de conocer los fototipos de piel, se debe conocer el PH del paciente para tomar una decisión y seguir -o no- los pasos específicos del […]
Ácidos y bases. Investigación virtual – Experimenta, aprende
[…] https://culturacientifica.com/2019/11/28/que-es-el-ph/ […]
Fanmascotas
Muy interesante. Yo soy biólogo y trabajo en el mundo de los acuarios y el pH del agua nos da mucha información acerca de cómo está el agua. Los pH bajos indican mucha materia orgánica o aguas negras. Por el contrario, los pH altos son indicativos de aguas duras en las que no todos los peces pueden vivir pero sí son muy aptas para los cíclidos africanos o los peces marinos. Gracias por el post. Saludos.
¿Cómo lavar los peluches de Knitabuddy? – Knitabuddy – Peluches y mordedores artesanales
[…] como para el algodón de los peluches. Otra buena razón para emplear este tipo de producto, es que su PH es muy parecido al de nuestra piel, y además no tiene perfumes añadidos que puedan resultar […]
El valor del pH en un secante – Mucho mas que un secante
[…] higienizante tienen un poder de absorción y su función antiséptica viene determinada por el pH. La importancia de este valor se da en múltiples ámbitos del uso de productos (limpieza, higiene, alimentación, etc…). A lo largo de la historia ha […]
LA VERDAD SOBRE EL DIOXIDO DE CLORO 2021
[…] El pH es una manera de medir la acidez o basicidad de una solución acuosa gracias a una escala. Si quieres ampliar más conocimientos sobre este tema te dejamos un artículo que lo explica bastante bien. […]
Sistemas de hidroponía en cultivos de cannabis medicinal | Inveurop
[…] considera que el agua tiene un pH «neutro» de 7 y al cannabis generalmente le gusta vivir en un entorno de pH entre 5 y 6. Los valores de pH […]
Agua de piscina transparente ¿Cómo mantenerla? – Cool Pool
[…] que la piscina tenga el agua limpia. Para ello, los niveles que debe mantener el agua en su pH son de 7,2 hasta 7,6. Para conocer exactamente estos valores, en el mercado hay medidores de pH […]
Olvido Fuentes Rojas
Excelente artículo! De una claridad específica, de muy fácil comprensión, con una percepción de sensaciones muy intuitivas. Se agradece todo el tiempo invertido!
7 consejos para mantener adecuadamente la piscina – Cool Pool
[…] también deberás cerciorarte de que el pH se mantenga entre 7.2 y 7.8. Cuánto más bajo sea el pH dentro del límite indicado, menor cantidad de cloro se necesitará. En cambio, cuanto más elevado […]
Jabón de cuaba: Datos curiosos que no sabías
[…] jabón de cuaba es un jabón con un contenido alcalino muy elevado, de hecho, tiene un pH de 11, muy alejado de lo que se conoce como un jabón […]
Limnobium laevigatum, una planta flotante sencilla.
[…] las he tenido en pH ácido y neutro. Es decir de 7,5 a 6. Hay aficionados que las mantienen en pH más ácidos y no tienen […]
Alimentos Alcalinos: ¿Qué son y cuáles son sus beneficios?
[…] alimentos alcalinos son aquellos que regulan el hidrógeno de nuestro cuerpo y ayudan a mantener un pH equilibrado en nuestro organismo. Cuando tomamos un alimento, este produce una reacción alcalina o acidez en […]
Poros dilatados: Remedios caseros para reducirlos – Expresion Sonora Noticias
[…] por sus propiedades antimicrobianas, además de eso ayuda en el control del acné. Restaura el pH en el cutis y ayuda a disminuir los poros […]
¿Por qué las fresas son de color rojo? – COP19
[…] antocianinas son conocidos los pigmentos presentes en las fresas, los cuales son sensibles al pH, y que pueden aparecer rojo-rosa en los ambientes ácidos, mientras que en los ambientes neutros lo […]
Poros dilatados: Remedios caseros para reducirlos – remedios y curiosidades
[…] por sus propiedades antimicrobianas, además de eso ayuda en el control del acné. Restaura el pH en el cutis y ayuda a disminuir los poros […]
Aprende Cómo Limpiar Anillos De Plata De Forma Fácil
[…] 1. Reacciones redox Te explicamos qué son las reacciones redox, los tipos que existen, sus aplicaciones, características y ejemplos de reacciones redox. concepto.de 2. Componentes de los dentífricos La mejor manera de valorar qu dentfrico escoger para el uso personal es conocer cules son sus principales componentes o agentes activo http://www.sanitas.es 3. ¿Qué es el pH? A menudo en cosmética se hace referencia al pH. También en productos de limpieza e higiene, y en alimentación. Incluso hay dietas anticientíficas, como la dieta alcalina, que dicen fundamentarse en el concepto de pH. culturacientifica.com […]