Descifrando el código de los materiales

¿Alguna vez os habéis preguntado por qué el cobre conduce la corriente eléctrica y el vidrio no? ¿Por qué el diamante es tan duro y el grafito de los lápices tan blando, aunque ambos estén compuestos de carbono? La respuesta no se encuentra a simple vista.
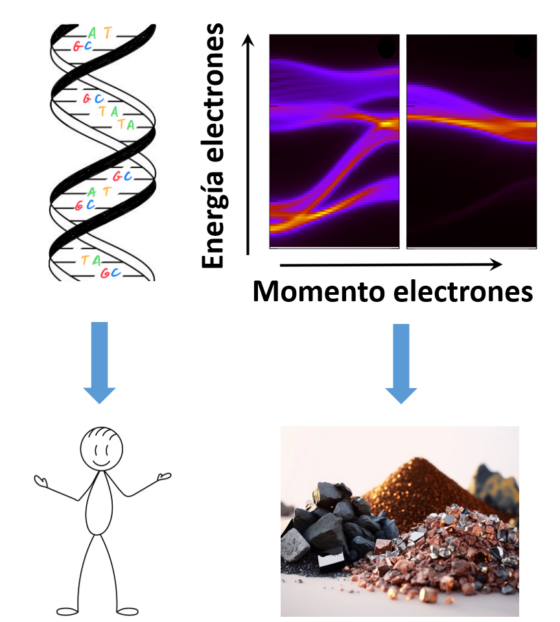
Pensemos en el ADN. El orden específico de las bases nitrogenadas del ADN codifica las peculiaridades de cada ser vivo. Nuestro código genético determina, por ejemplo, el color de nuestros ojos. De manera similar, cada material posee una distribución interna de sus electrones característica, conocida como “bandas de energía”, que dicta su comportamiento y condiciona propiedades tan importantes como su capacidad para conducir corriente o para imantarse, su reactividad química, o como veremos a continuación, su color.
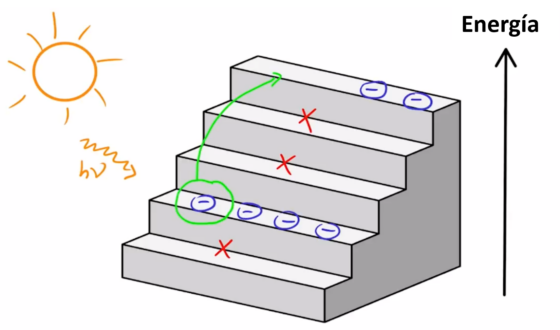
Imaginemos un material como una enorme escalera, donde cada peldaño corresponde a niveles de energía de sus electrones. Aquí es crucial el papel de la física cuántica. Sabemos que los electrones pertenecen a la clase de partículas conocidas como fermiones. El físico Wolfgang Pauli formuló para ellos el “principio de exclusión”, según el cual dos fermiones pertenecientes a un mismo sistema no pueden encontrarse en el mismo estado. Por otro lado, también necesitamos algo de física clásica. Los electrones poseen carga electrostática, por lo que están sujetos a la ley de Coulomb, que establece que las cargas de signo opuesto se atraen y las de igual signo se repelen. Los electrones, por tener carga negativa, son atraídos por los núcleos de los átomos, de carga positiva, a la vez que son repelidos por los demás electrones presentes en el material. Al hacer balance de todas estas normas, el resultado que obtenemos es que los electrones no pueden estar en cualquier nivel de energía del material: algunos niveles están prohibidos.
Así, la estructura de bandas electrónicas de cada material es su «ADN» o seña de identidad, formada por una combinación específica de niveles de energía permitidos y prohibidos, que condicionará sus principales propiedades. Por ejemplo, esta combinación específica determina si un material conduce bien la electricidad, como los conductores, si no deja fluir la corriente eléctrica, como en los aislantes…o incluso si la conduce sin resistencia ni pérdida de energía, el caso de los superconductores.
La aplicación de las leyes de la mecánica cuántica nos permite ir más allá y predecir cómo responderá un material ante la aplicación de un estímulo externo, como puede ser una presión mecánica, un campo magnético, o algo tan común como la luz. En semiconductores y aislantes, al absorber luz de una determinada longitud de onda, los electrones son “excitados”, lo que significa que pueden saltar a peldaños vacíos de mayor energía. Este tipo de proceso determina el color con el que vemos el material. Asimismo, se puede dar el proceso contrario de “desexcitación» de electrones, mediante el cual el material emite luz de una determinada longitud de onda en función de los peldaños descendidos. La tecnología LED, presente en muchos de los dispositivos que usamos diariamente, aprovecha este fenómeno de emisión de luz.

En un laboratorio podemos medir experimentalmente la estructura de bandas de los materiales a partir de la observación del resultado de excitar los electrones con distintas fuentes de luz, en particular de rayos-X y luz ultravioleta (UV). Pero si queremos ser realmente precisos al realizar nuestra “radiografía del material», debemos emplear la intensa luz procedente de radiación sincrotrón, que solo se encuentra disponible en instalaciones especiales. Entre ellas destaca el sincrotrón ALBA, situado en la provincia de Barcelona.


También podemos calcular la estructura de bandas empleando software de simulación basado en las llamadas teorías “ab initio”. Estas simulaciones reproducen el comportamiento de los electrones del material a partir de una serie de ecuaciones matemáticas formuladas a partir los dos fundamentos físicos descritos anteriormente: la mecánica cuántica y la ley de Coulomb. Se trata de cálculos tan complejos, que a veces requieren el uso de supercomputadores.
Finalmente, los físicos experimentales y teóricos colaboramos estrechamente para combinar nuestros hallazgos y así descodificar la estructura de bandas del material. Gracias a estas investigaciones, podemos diseñar y fabricar materiales con las propiedades específicas que deseemos.
Sobre las autoras: Maider Ormaza y Maria Blanco, profesoras investigadoras de la Facultad de Química de la Universidad del País Vasco/Euskal Herriko Unibersitatea
La Facultad de Química de la UPV/EHU cumple este año 50 años. Con motivo de este aniversario se han organizado un gran número de actividades festivas, de orientación del alumnado de secundaria, investigación, transferencia y divulgación. Entre estas últimas podemos encontrar “12 meses – 12 temas”, conjunto de actividades que pretende mostrar a la sociedad las temáticas desarrolladas en la Facultad. Entre estas actividades podemos encontrar el ciclo de charlas “50 años difundiendo la química”, en Ernest Lluch Kulturetxea, así como vídeos de divulgación, entrevistas en radio y artículos en los blogs de divulgación de la Cátedra de Cultura Científica. Durante todo el año contaremos con invitados especiales, como los cuatro Centros de Investigación nacidos de la Facultad (CIDETEC, CFM, DIPC y POLYMAT), así como los Premios Nobel Albert Fert y Jean Marie Lehn. Se puede consultar el conjunto de actividades programadas en la página web de nuestro 50 Aniversario.


José A.
Los electrones solamente pueden estar en los niveles permitidos. Pero pueden saltar de uno a otro. ¿Y durante el salto? ¿Se produce el salto en tiempo cero? ¿Se viola la imposibilidad de «estar» en zonas intermedias? En resumen ¿cómo se produce el salto?
Gracias.
María Blanco
El salto se produce cuando el electrón se estimula con la energía adecuada, en el sentido de que esa energía debe poder salvar los escalones prohibidos o «gap» de energía. Por ejemplo, si empleamos luz como estímulo, esto es, unas partículas llamadas fotones que interactuarán con los electrones, nos tenemos que fijar en su longitud de onda. El inverso de la longitud de onda es proporcional a la energía de esos fotones. Además de esa condición sobre la energía de los fotones, la interacción electrón-fotón sólo se dará con una cierta probabilidad: imagina que el fotón no siempre acierta a golpear al electrón. Todo esto se computa con una fórmula conocida como «la regla de oro de Fermi».
El electrón nunca está en niveles de energía prohibidos. Por las leyes cuánticas, está a la vez en el escalón incial y el escalón final mientras dure el estímulo. Si entretanto hacemos repetidamente un experimento capaz de determinar en cuál de los escalones está el electrón, obtendremos uno u otro resultado, escalón incial o final, con una probabilidad dictada por la regla de oro.