Hielo cuadrado por doquier

Este texto es una colaboración del Cuaderno de Cultura Científica con Next
Si nos preguntan a qué temperatura el agua se convierte en hielo, lo más normal es que respondamos que a cero grados Celsius (si la presión es la atmosférica). Si, siguiendo con el interrogatorio, la pregunta es ahora cuál es la geometría del hielo, es posible que recordemos la forma de los copos de nieve y respondamos que hexagonal. Ambas respuestas parecen bastante sólidas a la vista de nuestra experiencia habitual con el agua sólida. Y sin embargo, siendo correctas, ocultan una realidad mucho más compleja, extraña y fascinante.
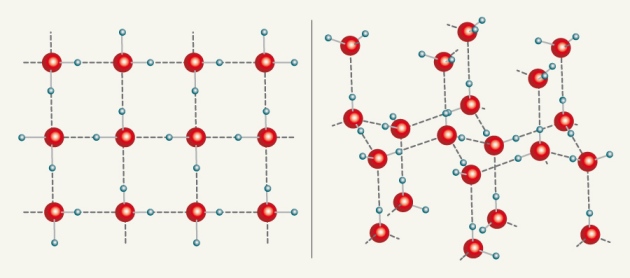
Acaba de publicarse en Nature un trabajo de un grupo de investigadores encabezado por Gerardo Algara-Seller, de la Universidad de Ulm (Alemania), y en el que participa el premio Nobel Andre Geim, de la Universidad de Manchester (Reino Unido), según el cual si ponemos agua entre dos capas de grafeno el agua se convierte en hielo ¡a temperatura ambiente! No solo eso, sino que este hielo tiene una estructura cristalina nunca vista hasta ahora en el agua: forma cristales bidimensionales perfectamente cuadrados. Esta nueva fase cristalina podría explicar algunos fenómenos extraños que se habían detectado trabajando con nanomateriales y, quizás, el de algunos sistemas biológicos.
Hasta ahora se conocían 17 fases estables distintas del hielo (16 cristalinas y una amorfa), cada una con su disposición molecular característica, su empaquetamiento y su simetría (o ausencia de ella). El nuevo hielo cuadrado no se parece a ninguna de ellas.
Los materiales en general se comportan de forma diferente a escala nanométrica. El comportamiento del agua es especialmente interesante porque está en todas partes en el planeta Tierra; incluso en el desierto de Atacama, uno de los lugares más secos del planeta, el agua cubre la superficie de los cuerpos aunque solo sea con unas pocas moléculas de espesor. Por esa misma razón es esperable encontrar agua en cualquier poro microscópico, salvo que se tomen medidas realmente excepcionales para impedir que esto sea así.
Durante décadas los científicos han intentado comprender la estructura y el comportamiento del agua que se encuentra confinada en esos espacios tan pequeños. La teoría sugiere multitud de nuevas fases posibles, pero no había sistemas de imagen lo suficientemente potentes para determinar la estructura cristalina a esa escala. Solo cabía recurrir a simulaciones por ordenador que no siempre proporcionan resultados consistentes.
Cuando intentas formar un bocadillo de agua usando dos láminas de grafeno como panes, pasa lo mismo que si intentas hacer un bocadillo de un buen pegote de mayonesa: la mayor parte escapa del bocadillo, a poco que hagas presión. En este caso las responsables de expulsar al agua son las fuerzas de van der Waals, y entre las capas de grafeno queda una proporción muy pequeña de agua. Como el grafeno es transparente a los microscopios electrónicos y, por otra parte, es tan hidrofóbico que no interacciona con el agua, los investigadores pudieron usar un microscopio electrónico de transmisión para ver el oxígeno de las moléculas de agua. Este procedimiento puso de manifiesto que las moléculas de agua estaban dispuestas de forma regular (algo característico de una fase sólida cristalina, esto es, hielo) siguiendo un patrón cuadrado.
Siendo este hallazgo sorprendente, no lo fue menos comprobar mediante simulaciones por ordenador, que el hielo cuadrado puede ser mucho más común de los que se piensa y que su formación no dependería de la composición química exacta de los nanoporos donde se encuentre. Puede que exista hielo cuadrado en cada poro microscópico que haya en cualquier material.
Estos descubrimientos podrían facilitar nuestra comprensión del flujo del agua a través de los canales, naturales y artificiales, en la nanoescala. Esto incluye por ejemplo a las acuaporinas, unas proteínas en las membranas de las células que se encargan del transporte del agua, y a los nanotubos de carbono. Aparte del aspecto teórico, esta mejor comprensión podría llevar a una mejora en la eficiencia de las tecnologías de filtrado, desalinización y destilación.
Referencia:
Algara-Siller G, Lehtinen O, Wang FC, Nair RR, Kaiser U, Wu HA, Geim AK, Grigorieva IV. (2015) Square ice in graphene nanocapillaries Nature DOI: 10.1038/nature.2015.17175
Sobre el autor: César Tomé López es divulgador científico y editor de Mapping Ignorance
Esta entrada participa en el XLVI Carnaval de Química alojado en el blog descubrirlaquimica2 de @descubrequimica.


descubrirlaquimica
Interesante artículo, eres la primera contribución del Carnaval de Química, enhorabuena
Hitos en la red #62 – Naukas
[…] es menos fina o el repertorio léxico más limitado, “cuadrao”. ¿De qué narices irá lo de Hielo cuadrado por doquier […]