Formación de micelas en fase gaseosa
¿Por qué el jabón disuelve la grasa? Porque, al mezclarse con el agua, sus moléculas forman unas estructuras esféricas llamadas micelas que recogen en su interior la grasa y la eliminan del medio. Un grupo de científicos de la Universidad del País Vasco/Euskal Herriko Unibertsitatea, de la Universidad de la Rioja y de la Universidad de Valladolid ha conseguido crear micelas sin necesidad de un entorno líquido y determinar con extremada precisión su estructura. La investigación ha ocupado la portada de la revista Angewandte Chemie, una de las más importantes en el campo de la Química.
Si miramos con un microscopio jabón en una mezcla acuosa, podríamos ver que el jabón crea unas macroestructuras totalmente ordenadas, formadas por numerosas moléculas que tienen dos partes, una polar y otra apolar. La parte polar es hidrofílica, por lo que queda rodeada por las moléculas de agua, que asimismo son polares, mientras que los grupos apolares, que son hidrofóbicos, se esconden entre otras moléculas de jabón interaccionando entre sí. Así aparecen esas estructuras globulares llamadas micelas, que conforman un entorno completamente diferente al del disolvente en el que se encuentran inmersas. Esta propiedad de formar micelas resulta crucial para los seres vivos y permite, por ejemplo, la existencia de las membranas celulares. También tiene usos farmacológicos, ya que un medicamento puede viajar «escondido» en el interior de las micelas protegido del entorno hasta ser liberado en la parte del organismo donde tiene que ejercer su función.
Entre las moléculas anfifílicas, esto es, aquellas que como el jabón tienen un extremo hidrofílico y el otro hidrofóbico y tienen la capacidad de formar micelas, se encuentra el propofol, un anestésico ampliamente utilizado en cirugía. Los investigadores, dirigidos por el Grupo de Espectroscopia de la UPV/EHU, han realizado su investigación con este anestésico, en fase gas, lo que permite seleccionar las moléculas sin interacciones de cualquier otra molécula del entorno. Emplearon para ello un complejo sistema experimental, que les permitió formar agregados de tamaño creciente de moléculas de propofol, y determinar sus parámetros estructurales mediante una combinación de técnicas espectroscópicas láser y cálculos mecano-cuánticos, llevados a cabo en los superordenadores de la Universidad del País Vasco (UPV/EHU) y de la Fundación i2BASQUE.
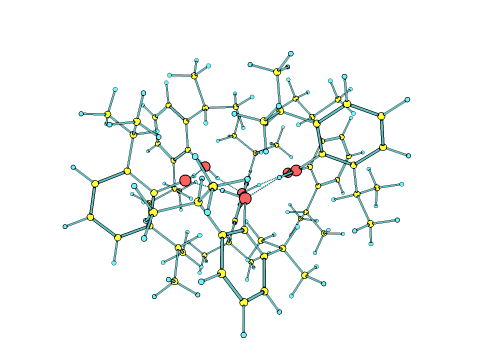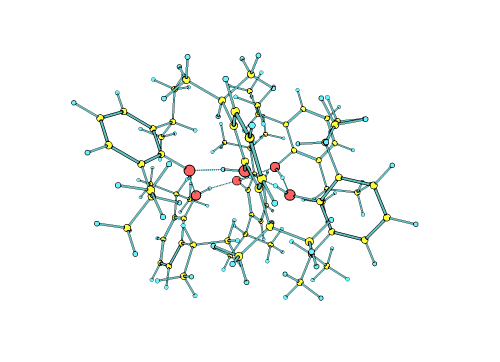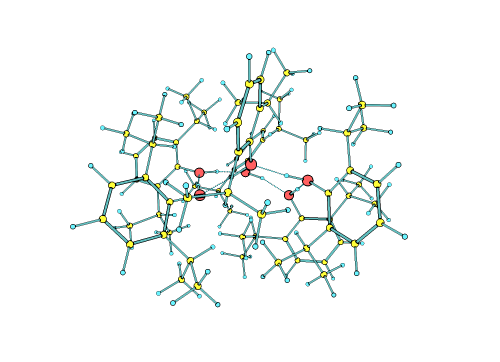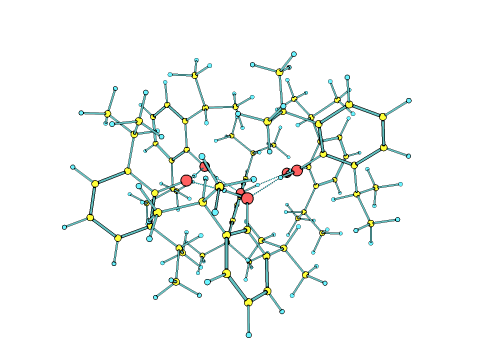
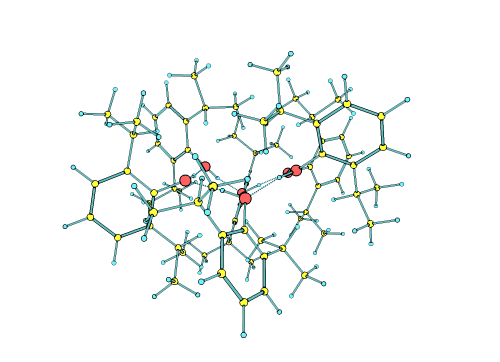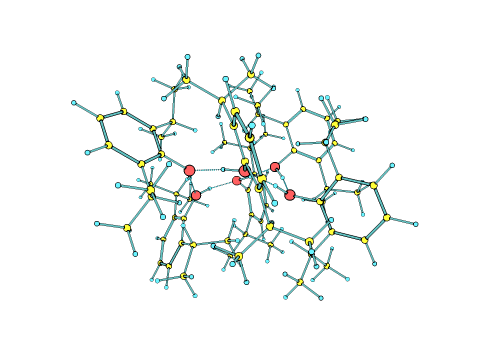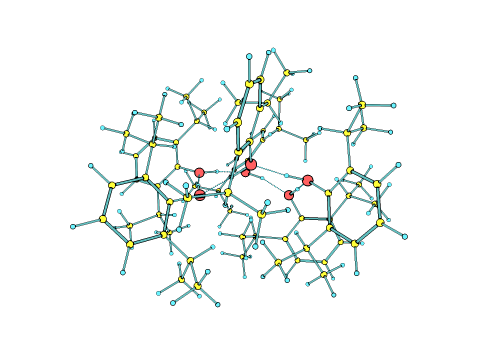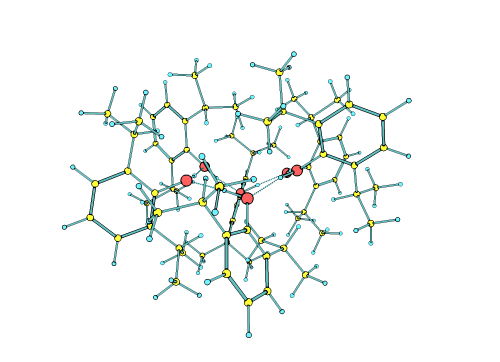
Los investigadores pudieron crear, aislar y finalmente determinar que las moléculas de propofol se autoorganizan, sin necesidad de estar en un entorno líquido, formando una estructura de micela inversa, es decir, con un núcleo hidrofílico estabilizado por enlaces de hidrógeno, y una envoltura hidrofóbica formada por la interacción de la parte apolar de todas las moléculas del propofol, estabilizada por fuerzas dispersivas. Las interacciones que forman las micelas inversas descritas en este trabajo son las mismas que gobiernan el plegamiento de las proteínas y la interacción entre moléculas biológicas, por lo que las conclusiones alcanzadas en este trabajo podrían ser extrapolables a otros sistemas biológicos relevantes.
«Si tenemos en cuenta que las micelas son una de las formas de autoorganización más primitivas y que las células son, al fin y al cabo, una estructura protegida por una capa exterior, podríamos aventurar que las micelas estarían relacionadas con la aparición de la vida sobre la tierra», señala el investigador de la Facultad de Ciencia y Tecnología José Andrés Fernández.
Referencia:
León, I., Millán, J., Cocinero, E. J., Lesarri, A. and Fernández, J. A. (2013), Shaping Micelles: The Interplay Between Hydrogen Bonds and Dispersive Interactions . Angew. Chem., 125: 7926–7929. DOI: 10.1002/ange.201303245
Esta anotación participa en el XXVII Carnaval de Química que organiza Educación química
Edición realizada por César Tomé López a partir de materiales suministrados por UPV/EHU Komunikazioa
José Manuel López Nicolás
Hola,
estupendo post y gran investigación. ¿Han determinado los autores algún método de determinar en estado gaseoso la concentración micelar crítica del propofol? Me refiero a aquella concentración a partir de la cual se forman micelas.
Gracias
José Andrés
Hola José Manuel, muchas gracias por tu comentario. Realmente, el proceso de creación de estas micelas en fase gas es distinto de la disolución. Hacemos pasar 2-3 atm de presión de una mezcla de propofol y Helio por una válvula pulsada que expande la mezcla dentro de la cámara de un espectrómetro de masas que se encuentra a alto vacío. De este modo, la mezcla se enfría y las moléculas se agregan. Si aumentamos la cantidad de propofol, por ejemplo, calentándolo, podemos regular la cantidad de moléculas en los agregados, pero siempre vamos a tener varias estequiometrías mezcladas. Si estás muy interesado, te puedo pasar copia del artículo.
José Manuel López Nicolás
Hola José Andrés,
pues estaría interesado. Mi primer paper publicado, allá por el año 1994, hablaba del fenómeno de agregación de de detergentes a través de micelas mixtas. Además añadíamos un agente encapsulante para modificar la c.m.c.
Mi mail es josemln@um.es.
Mil gracias
Jose
Formación de micelas en fase gaseosa | M…
[…] ¿Por qué el jabón disuelve la grasa? Porque, al mezclarse con el agua, sus moléculas forman unas estructuras esféricas llamadas micelas que recogen en su interior la grasa y la eliminan del medio. […]
Un tornado magnético para manipular la interfaz aire-agua — Cuaderno de Cultura Científica
[…] Formación de micelas en fase gaseosa […]