La tabla periódica en el arte: Arsénico
No diga veneno, diga arsénico. Pocos elementos químicos imponen tanto respeto como el arsénico. Lo usaron los Borgia para quitarse del medio a sus enemigos políticos y más de un noble para acceder a su herencia antes de tiempo. También ha servido para mandar al otro barrio a algún que otro marido y para dar de baja a todo tipo de personajes de novela negra. Pero si miramos más allá de su toxicidad, veremos que el arsénico es un elemento que ofrece un arcoíris de colores en forma de pigmentos.

Cuando el verde puede matar
El sueco Carl Wilhem Scheele ocupa un lugar de honor en el Olimpo de la química. Y eso que uno de sus más grandes descubrimientos no ha servido para granjearle muy buena fama. En 1775 sintetizó un pigmento de un agradable color verde más duradero que los carbonatos de cobre ampliamente utilizados hasta esa fecha. El proceso para lograrlo no era excesivamente complicado: calentar una disolución de carbonato de sodio en la que poco a poco se disolvía óxido de arsénico, añadir sulfato de cobre, recoger el precipitado que se formaba y calentarlo. Así se obtenía el verde de Scheele (principalmente CuHAsO3), un sólido que cambiaba de tonalidad según la proporción de cobre y arsénico.
Sin embargo, había un problema: la elevada toxicidad del arsénico. Según nos cuenta la historiadora Victoria Finley, el propio Scheele estaba al tanto del problema y en 1777 escribió a un colega preocupado porque pensaba que se debía alertar del peligro a los consumidores. Como con las cajetillas de tabaco, vamos. Sea como fuere, el producto salió al mercado al año siguiente y tuvo un éxito arrollador.

El éxito fue todavía mayor cuando, con el cambio de siglo, apareció un compuesto similar más estable (3 Cu(AsO2)2·Cu(CH3COO)2). En su preparación se empleaba ácido acético, pero la fórmula se mantuvo en secreto hasta que fue descubierta por un joven Justus von Liebig. Liebig y Scheele, dos grandes químicos unidos por el verde y por el arsénico. El pigmento tuvo muchos nombres: verde esmeralda, verde de París, verde Veronés, etc. Pero que sus evocadores nombres no nos dejen engañar. Si, además de usarse en pintura, sirve de raticida por algo será.
Estos nuevos pigmentos verdes no solo entusiasmaron a los prerrafaelitas y los impresionistas, sino que triunfaron como tinte para los vestidos de señora, para dar color a libros, velas y jabones y, especialmente, para colorear el empapelado de las casas. Ni en la más macabra trama urdida por Agatha Christie hubiera habido tanto arsénico. Ya en 1857 un doctor de Birmingham advertía en la prestigiosa The Lancet sobre los peligros del papel teñido de verde: “En una ocasión un niño chupó unas tiras de papel y apenas escapó con vida”.
Pero, ¿era necesario chupar el papel para envenenarse? En absoluto. Existen otras dos teorías para explicar el envenenamiento por el “empapelado asesino”. La primera apunta a que pequeñas partículas de pintura se descascarillaban y podían entrar en el sistema respiratorio como si fuesen motas de polvo. La segunda resulta mucho más interesante desde el punto de vista científico. En condiciones de humedad pueden aparecer ciertos mohos en la pared. Estos mohos, en su afán por sobrevivir a las altas cantidades de arsénico, lo metabolizan y forman compuestos orgánicos volátiles. De la pared al aire y del aire a los pulmones.
Podríamos recrearnos en el uso del arsénico como veneno y hablar de una de sus (supuestas) víctimas más ilustres: Napoleón. Por poético que resulte y por mucho que se repita, es muy poco probable que fuese este elemento quien asesinó Emperador. Dicho esto, hablemos de un tema más agradable: la pintura. Lo cierto es que se conocen pocas obras que contienen verde de Scheele. Básicamente porque la aparición al de poco tiempo del verde esmeralda le comió la tostada. Aun así, no podemos pasar por alto al más ilustre pintor de acuarelas de todos los tiempos: Joseph Mallord William Turner. Paradójicamente, la obra en la que se ha encontrado este pigmento es un óleo.

El verde esmeralda fue uno de los verdes más importantes del s. XIX como demuestra la lista de ilustres pintores que lo usó: Manet, Monet, Pisarro, Gauguin, etc. Pero si alguien destaca sobre todos los demás, ese es van Gogh. Entre 1888 y 1889 el pintor holandés mantuvo una producción frenética en Arles. Allí realizó varios retratos a la familia Roulin, cuyos miembros posaron sin descanso mientras el artista daba espesas pinceladas de verde esmeralda. ¡Qué pensarían Joseph, Augustine, Armand, Camille y Marcelle si les hubiesen dicho que sus rostros iban a colgarse en los museos más importantes del mundo!

El amarillo del rey
La palabra arsénico deriva de arsenikon que en griego significa viril o macho. No parece una etimología muy apropiada hasta que no se indaga un poco más. El vocablo griego proviene a su vez del persa zarnik donde encontramos la raíz que significa oro. Esto ya empieza a cobrar sentido. Ese es el nombre que se le daba un mineral compuesto por azufre y arsénico que tiene color dorado. Hoy en día lo llamamos oropimente (As2S3), del latin auripigmentum. De hecho, los alquimistas estaban convencidos de que contenía oro y trataron por todos los medios de extraer del mineral el más preciado de los metales. Obviamente, lo único que lograron fue algún que otro envenenamiento.
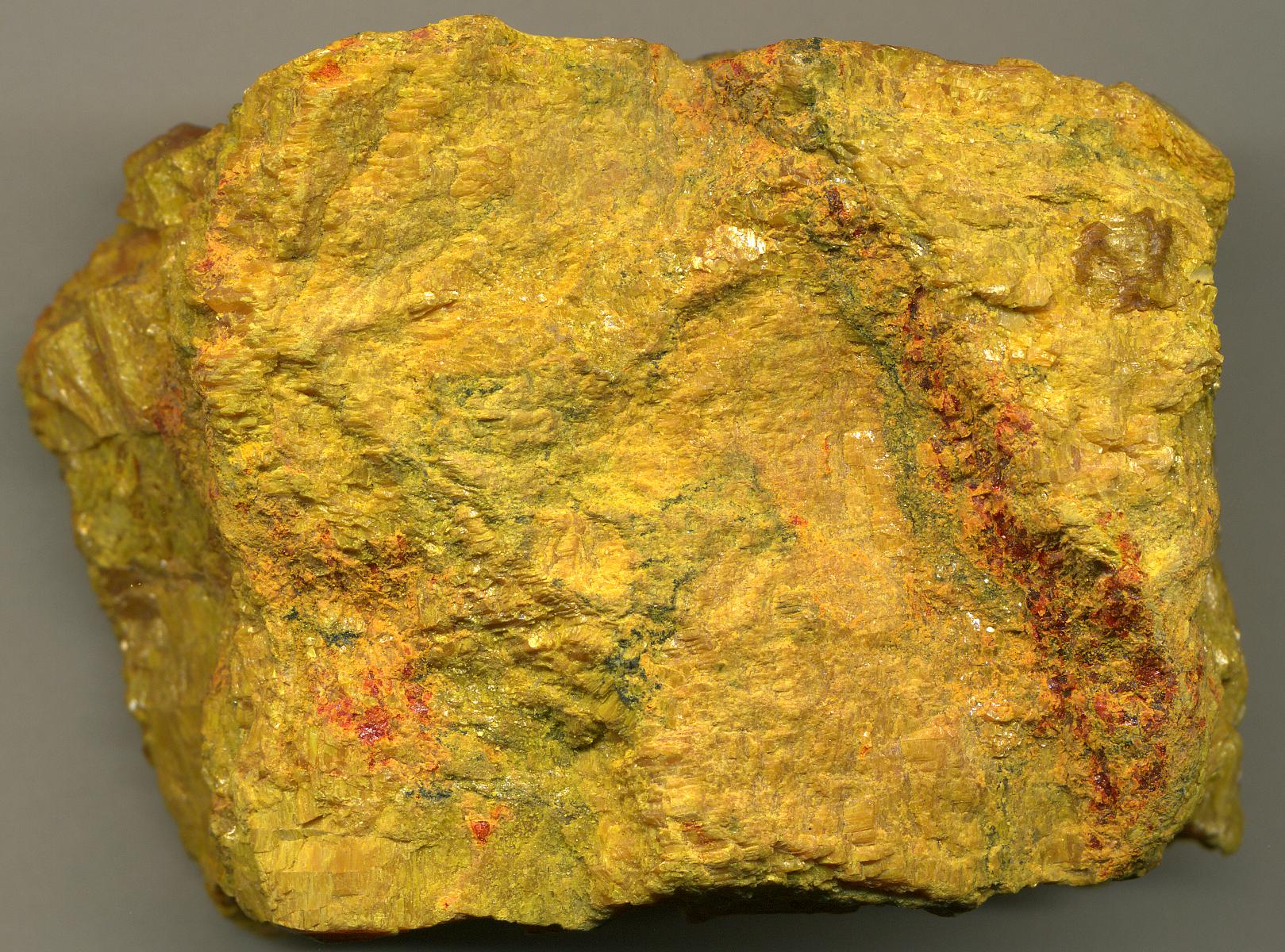
El oropimente tiene un color amarillo brillante que ha hecho que se emplee como pigmento desde los tiempos del Imperio Nuevo de Egipto (s. XVI a.e.c.). En cualquier caso, tampoco ha sido el amarillo más popular, quizás porque se ennegrece en contacto con muchos otros pigmentos o porque es muy venenoso. Si Scheele se preocupaba por la toxicidad de su verde en el s. XVII, Estrabón ya hablaba de los peligros del arsénico en época de Augusto. En su Geografía cuenta cómo hace 2000 años los condenados a trabajar en las minas de Asia Menor morían por culpa de la sandáraca. Hoy sabemos que se refería al oropimente o al rejalgar, del que nos ocuparemos más adelante. En la Edad Media también eran muy conscientes de que el oropimente debía ser tratado con respeto. Ya lo advertía Cennino Cennini en su indispensable Libro del Arte “Amarillo es un color que se denomina oropimente. Dicho color es artificial y hecho de alquimia; es realmente venenoso, y de una bella tonalidad amarilla que recuerda al oro”.
Este pasaje nos transporta inevitablemente a la manufactura del pigmento dorado. Pese a que se puede obtener de forma natural del mineral homónimo, desde época medieval se produce artificialmente. La mejor receta nos la dejó el químico y farmacéutico Robert Dossie en el s. XVIII. En ella explica cómo el arsénico en polvo debe mezclarse con flores de azufre en proporción de veinte a uno. Luego se calienta la mezcla para lograr la sublimación (pasar de sólido a gas) y se recoge el oropimente. Al parecer el pigmento logrado de forma sintética se conocía como amarillo del rey y era de mayor pureza. Recuerden, lo natural no tiene por qué ser mejor.
Aunque hemos dicho que este pigmento no ha sido excesivamente empleado a lo largo de la historia (occidental), hay unas cuantas obras de gran relevancia que podemos destacar. Para reflejar la variedad de técnicas y soportes en las que se ha empleado mencionaremos el singular libro de Kells en el Trinity Collegue (s. IX), el altar de Esquius en el Museo Nacional de Arte de Cataluña (s. XII) o las pinturas de la cúpula de la mezquita Al-Aqsa de Jerusalén (s.XIV).

Pero quedémonos con un óleo barroco que muestra cómo las obras de arte están vivas y cambian con el tiempo. Jan Davidsz. de Heem pintó una guirnalda con frutas y flores en la segunda mitad del s. XVII que hoy podemos disfrutar en el Rijksmuseum de Amsterdam. Bajo la granada que muestra su apetitoso contenido cuelga un cítrico con un aspecto poco atractivo. Los análisis químicos nos han permitido saber que posiblemente el fruto fuese de un color mucho más vivo y brillante, no en vano estaba pintado con oropimente. Pero este pigmento se puede degradar a óxidos de arsénico y desvanecerse. Al analizar las diferentes capas de la pintura se observó que los óxidos habían penetrado hacia el interior del cuadro y habían reaccionado con el plomo de otros pigmentos. Todo ello dio como resultado una especie de limón que ha madurado en exceso.

El polvo de la cueva
El oropimente tiene un primo de color naranja y composición química similar conocido como rejalgar (As4S4, As2S2 o AsS). Con dicho nombre sólo puede tener origen árabe: ráhǧ alḡár “polvo de la mina”. No en vano, al igual que el oropimente, es un mineral natural que, como decíamos antes, los romanos llamaban sandáraca. Posiblemente por el parecido, esta palabra se usa hoy para una resina de color rojizo en un caprichoso cruce etimológico entre dos materiales artísticos.

El rejalgar ha tenido un papel menos importante que el oropimente en la Historia del Arte, así que podemos decir que es el primo pobre. Incluso hay quien lo llamaba oropimente quemado, como si no tuviese entidad para tener su propio nombre. Eso no quiere decir que no haya tenido su momento de gloria. En China se usaba con frecuencia y en Persia e India, por ejemplo, se empleó en la elaboración de manuscritos. De hecho, en la medicina oriental tuvo un importante rol en medicina. Será por aquello de que lo que no te mata te hace más fuerte.
Dado que oropimente y rejalgar están inevitablemente unidos, pondremos el broche final a este artículo con una obra maestra en el que ambos pigmentos conviven en armonía. Se trata del retrato de Vincenzo Morosini realizado por Tintoretto, uno de los grandes exponentes de la escuela veneciana. Aquella en la que el color lo dominó todo. Y para colores los del arsénico, que además de los pigmentos verdes, amarillos y naranjas que acabamos de ver, está presente en el azul esmalte y en el violeta de cobalto.

Para saber más:
E. West FitzHugh. Artist’s Pigments: A Handbook of Their History and Characteristics. (Volume 3). National Gallery of Art (1998).
N. Eastaugh, V. Walsh, T. Chaplin y R. Siddall. Pigment Compendium: A Dictionary and Optical Microscopy of Historic Pigments. Routledge, Londres (2008).
V. Finlay. Colores. Editorial Océano, Barcelona (2004).
Sobre el autor: Oskar González es profesor en la facultad de Ciencia y Tecnología y en la facultad de Bellas Artes de la UPV/EHU.

Carmen González Martín
Muchas gracias por el artículo. Soy profesora de Toxicología y me ha resultado interesantísimo