Viendo a los electrones moldear las reacciones químicas
Imagina capturar en una fotografía un momento efímero: el movimiento de un electrón durante una reacción química. Desde los albores de la química moderna, la idea de «ver» cómo se desplazan estas partículas subatómicas parecía un sueño imposible, o en todo caso, el capricho de un novelista de ciencia ficción poco riguroso. Sin embargo, un equipo dirigido por Ian Gabalski, de la Universidad de Stanford, ha logrado un avance decisivo para convertirlo en realidad. Su estudio demuestra por primera vez que es posible observar directamente la dinámica de los electrones de valencia —aquellos que participan activamente en las reacciones químicas— en tiempo real.

¿Por qué es tan complicado observar los electrones de valencia?
Las reacciones químicas se inician cuando los electrones más externos de los átomos, conocidos como electrones de valencia, se reorganizan: rompen enlaces existentes y forman nuevos. Estos electrones determinan cómo comienza una reacción y qué productos finales se obtienen. El desafío radica en que, en experimentos con rayos X, los electrones internos —los más cercanos al núcleo atómico y no involucrados en las reacciones— dominan la señal detectada, eclipsando las sutiles variaciones producidas por los electrones de valencia.
¿Cómo lo han logrado?
El secreto reside en el uso de pulsos de rayos X ultracortos, cada uno de aproximadamente 30 femtosegundos (30 × 10⁻¹⁵ segundos), generados por el Linac Coherent Light Source (LCLS) en el Laboratorio Nacional de Aceleradores SLAC, en California.
El experimento comienza con un pulso de luz ultravioleta que excita una molécula de amoníaco (NH₃)*, alterando su geometría: de una estructura piramidal pasa a una planar. Esta transformación facilita que uno de los tres átomos de hidrógeno se desprenda, llevándose consigo un electrón de valencia que formaba parte del enlace. Dado que el hidrógeno no posee electrones internos (su único electrón es de valencia), este proceso deja expuesta la dinámica de los electrones de valencia sin la interferencia de señales de electrones centrales.
Inmediatamente después, el pulso de rayos X incide sobre la molécula. Los fotones de rayos X se dispersan en ángulos que dependen de la distribución espacial de los electrones (la densidad electrónica). Al capturar estos fotones dispersados en un detector bidimensional, los investigadores reconstruyen una «instantánea» de la densidad electrónica en ese momento preciso.
Dos caminos distintos
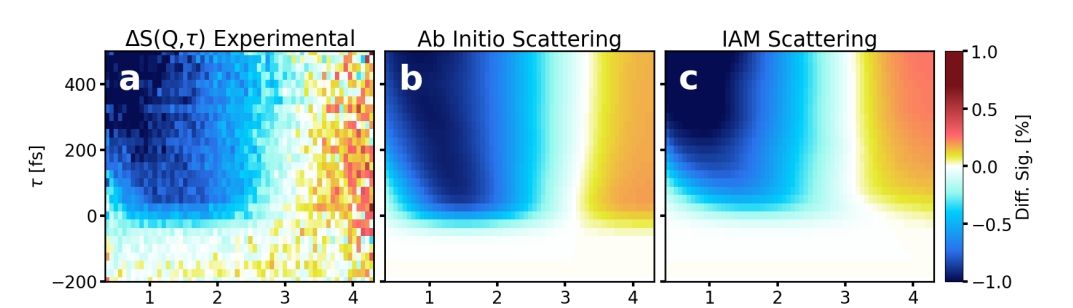
Gracias a esta técnica, el equipo identificó dos vías diferentes por las que el átomo de hidrógeno puede separarse de la molécula. En cada vía, la densidad de los electrones de valencia —es decir, la «forma» probabilística de su distribución en el espacio— era única. Estas diferencias se mantuvieron durante más de 200 femtosegundos. Al comparar los resultados experimentales con simulaciones cuánticas detalladas, los científicos confirmaron que estaban capturando con precisión la evolución de los electrones de valencia a lo largo de la reacción.
Comparación con otras técnicas
Una alternativa para generar «películas moleculares» es la difracción electrónica ultrarrápida, que emplea electrones de alta energía en lugar de rayos X como sonda. Este método permite visualizar estructuras atómicas en movimiento, pero su resolución temporal es inferior: típicamente superior a 50 femtosegundos. En contraste, la dispersión de rayos X ultrarrápida ofrece una vista más nítida y veloz de la dinámica electrónica, acercándose incluso a resoluciones por debajo de 10 femtosegundos.
¿Qué implicaciones tiene este avance?
Este logro permite visualizar directamente cómo la dinámica de los electrones de valencia influye en el desarrollo de una reacción química. Hasta ahora, solo podíamos inferir estos movimientos mediante modelos teóricos —como una película imaginaria en nuestra mente—, pero ahora estamos empezando a obtener imágenes reales que la materializan.
Mediante esta combinación innovadora de pulsos láser ópticos y rayos X ultrarrápidos, estamos penetrando en el mundo microscópico para observar cómo los electrones actúan en tiempo real durante una reacción. Es como fotografiar el delicado ritmo de un enlace químico en transformación: lo que antes era invisible, ahora emerge y se deja capturar. Estos conocimientos podrían revolucionar el diseño de procesos industriales más eficientes y sostenibles, medicamentos más precisos o materiales con propiedades inéditas.
Los retos futuros
El próximo objetivo es alcanzar resoluciones temporales en la escala de attosegundos (10⁻¹⁸ segundos) para estudiar fenómenos aún más fugaces, como la migración de cargas o el movimiento correlacionado de electrones. Esto parece factible gracias al desarrollo de fuentes de rayos X de attosegundos en instalaciones como el LCLS-II en Estados Unidos o el European X-Ray Free-Electron Laser en Alemania. Otro desafío es extender estas técnicas a moléculas más complejas, donde los electrones internos podrían seguir ocultando señales, posiblemente mediante detectores que discriminen energías para aislar las contribuciones de los electrones de valencia.
(*) Nota: Siendo estrictos, amoniaco deuterado, esto es, amoniaco en el que los tres hidrógenos son deuterios.
Referencia:
Ian Gabalski et al (2025) Imaging Valence Electron Rearrangement in a Chemical Reaction Using Hard X-Ray Scattering Phys. Rev. Lett. doi: 10.1103/53h3-vykl
Sobre el autor: César Tomé López es divulgador científico y editor de Mapping Ignorance
