En busca del compuesto perdido
La Facultad de Ciencias de Bilbao comenzó su andadura en el curso 1968/69. 50 años después la Facultad de Ciencia y Tecnología de la UPV/EHU celebrará dicho acontecimiento dando a conocer el impacto que la Facultad ha tenido en nuestra sociedad. Durante las próximas semanas en el Cuaderno de Cultura Científica y en Zientzia Kaiera se publicarán regularmente artículos que narren algunas de las contribuciones más significativas realizadas a lo largo de estas cinco décadas. Comenzamos con la serie “Espectrometría de masas”, técnica analítica que supone el ejemplo perfecto del incesante avance de la Ciencia y la Tecnología.
Las series de policías e investigadores han puesto en nuestras vidas el laboratorio científico y con él, la espectrometría de masas. La realidad es algo diferente a la ficción, pero en ambos casos es cierto que la espectrometría de masas es una técnica muy habitual cuando se trata de buscar moléculas, tanto si sabemos lo que estamos buscando como si no.
Pondré un ejemplo en el que la espectrometría de masas ha sido una técnica clave. Todos sabemos que está prohibido conducir bajo los efectos de sustancias estupefacientes. En caso de sospecha o simplemente en un control rutinario se realiza un test “in situ”. Se toma una muestra de saliva y mediante una reaccion enzimática (inmunoensayo) se obtendrá un resultado positivo o negativo. En ocasiones, moléculas similares a las buscadas pero que podrían no estar prohibidas presentan reactividades cruzadas, por lo que los resultados positivos se confirman en el laboratorio, principalmente mediante espectrometría de masas. En estos casos es importante corroborar la identidad de la molécula (lo que se conoce como análisis cualitativo). En segundo lugar, se procede al análisis cuantitativo, es decir, a calcular la concentración del compuesto en el organismo.
¿Pero qué sucede si el resultado del primer test es negativo, pero el comportamiento del individuo indica claramente el consumo de algún tipo de droga? En este caso hay que poner a trabajar la mente y la maquinaria científica.
Hace algunos años, irrumpieron en el mercado unas mezclas de plantas, declaradas como incienso, que fumadas, provocaban efectos similares a los del cannabis (Imagen 1). A pesar de que la policía había detectado el consumo de estos productos, no se encontraban en ellos ninguna de las drogas incluídas en los analísis de rutina de los laboratorios de toxicología forense. Después de que un par de adolescentes acabaran en urgencias estaba claro que teníamos que cambiar la estrategia de búsqueda.

En la mayoría de los laboratorios de toxicología los análisis de basan en una estrategía de tipo dirigido (“target”), es decir, sólo se ve lo que se busca. Traducido al idioma de la espectrometría de masas significa que el instrumento solo registra las relaciones masa/carga (m/z) que nosotros hayamos incluído en el método de análisis. Para todo lo demás, el instrumento es ciego. Esta es la principal desventaja de esta estrategia. La principal ventaja es la sensibilidad, es decir, así alcanzamos a detectar compuestos en concentraciones más bajas y evitar falsos resultados negativos.
Punto uno: abrir horizontes
Partiendo de la base de que se nos estaba escapando algo, conseguimos concentrar una muestra del extracto de las plantas y utilizamos un modo de análisis no dirigido con el que, gracias a la espectrometría de masas, pudiésemos encontrar compuestos que el modo dirigido nos impedía ver.
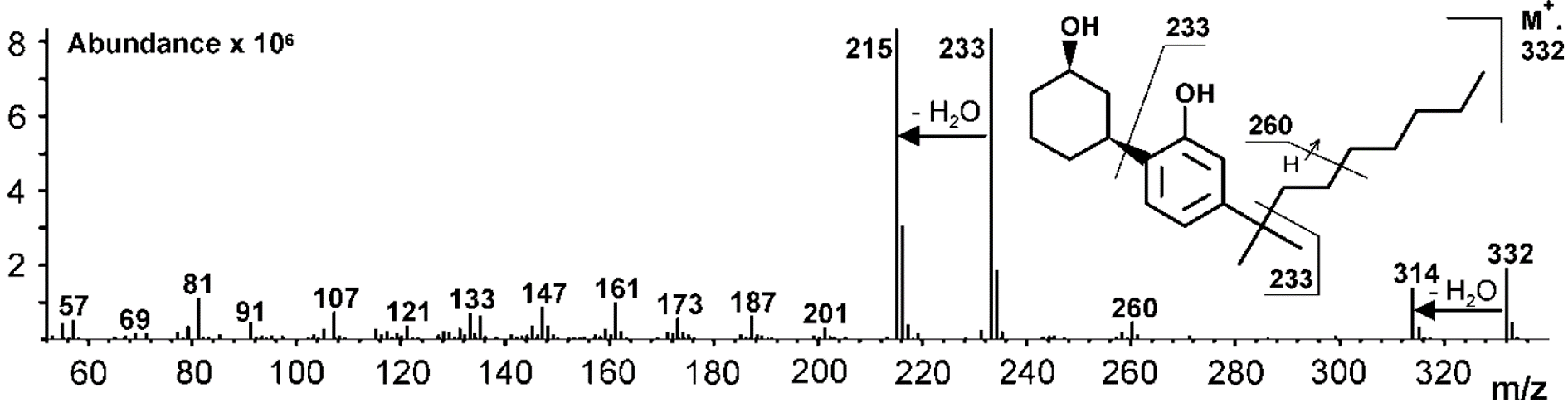
Comparando los espectros de masas, que son como la huella dactilar de una molécula (Imagen 2). pudimos identificar algunos de los compuestos mayoritarios. Para otros, en cambio, fue necesario usar información complementaria como la resonancia magnética nuclear. Gracias a estos análisis, se pudo comprobar que en esa mezcla de incienso había cannabinoides sintéticos, que en muchos casos habían sido desarrollados por la industria farmaceútica, pero no habían llegado al mercado de los medicamentos por diferentes razones. Estas sustancias producen efectos similares a los del cannabis pero no estaban incluídas en ninguna base de datos y por eso pasaban totalmente desapercibidas en los análisis rutinarios. Además, no existían datos sobre toxicidad o efectos secundarios.
Punto dos: definir nuevas metas
Una molécula interactúa con su receptor mediante una unión de tipo llave-cerradura. Esto quiere decir que, conociendo la parte estructural que interactúa con el receptor, se pueden realizar cambios en el resto de la molécula manteniendo su función. En este principio se basa el desarrollo de fármacos y la mayoría de modificaciones van destinadas a aumentar la solubilidad, la permeabilidad o mejorar la farmacocinética. Sin embargo, en el caso de los cannabinoides sintéticos usados en estos “inciensos”, esos cambios consiguen que, manteniendo el efecto sobre el sistema nervioso central, las moléculas no sean detectadas en los análisis rutinarios. El peligro de estas modificaciones radica en la posibilidad de potenciar los efectos centrales de estas sustancias y en la falta de estudios toxicocinéticos. Y aquí vuelve a entrar en juego la espectrometría de masas. Es necesario cuantificar estas sustancias y correlacionar estas concentraciones con los efectos que experimentan los consumidores.
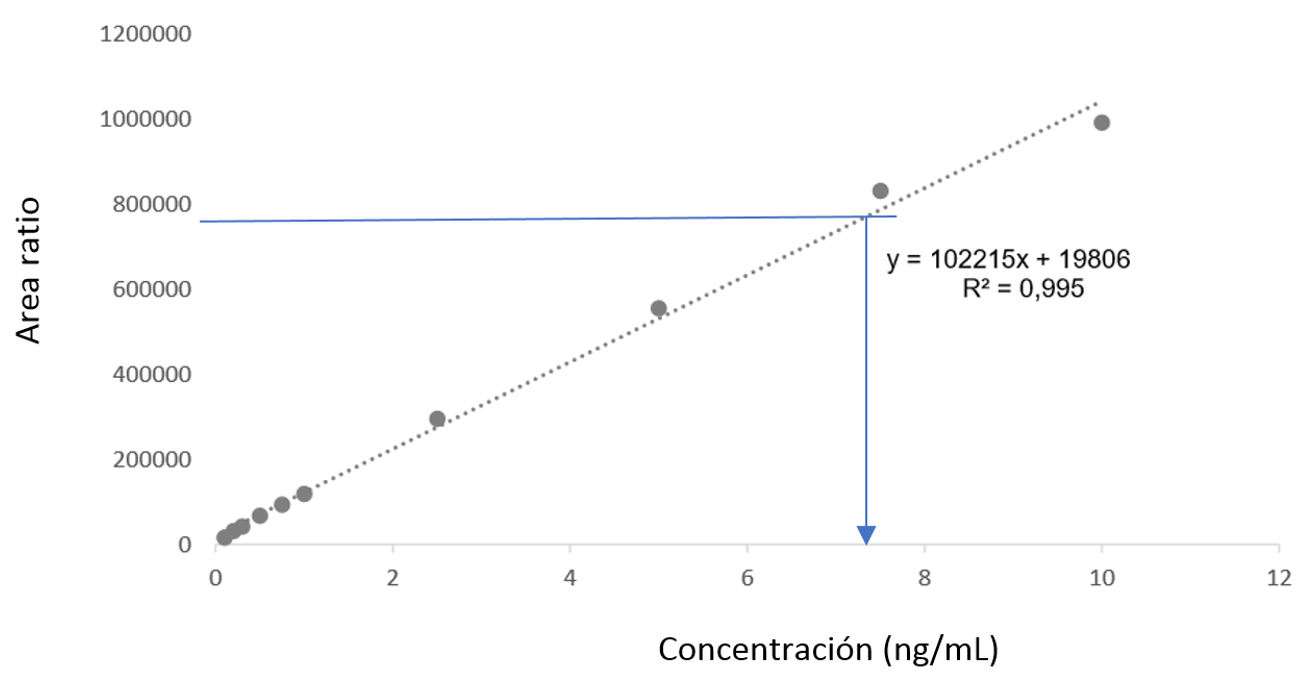
Para poder calcular la concentración de un compuesto es necesario construir una curva de calibrado. En ésta se representa gráficamente la señal obtenida para una seria de muestras en función de la concentración del compuesto en esas muestras (que nosotros hemos elegido y preparado). En espectrometría de masas la construcción de la curva de calibrado es un poco más compleja, ya que es necesaria la adición de otra sustancia (el estándar interno) para corregir efectos de la técnica. Así, conociendo la señal obtenida para una muestra de concentración desconocida se puede obtener el valor de su concentración (flecha azul). En el caso de los cannabinoides sintéticos, calcular las concentraciones es una forma de relacionar dosis y efectos de estas sustancias en el organismo y evaluar su perfil toxicocinético, es decir, a partir de qué concentraciones comienzan los efectos tóxicos y con qué velocidad el cuerpo humano es capaz de eliminarlos del organismo.
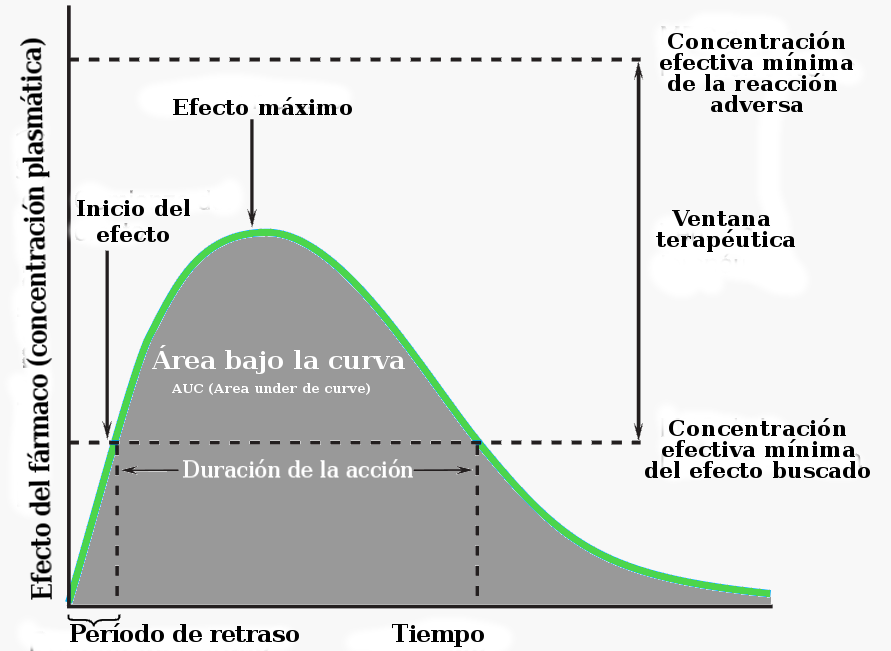
La espectrometría de masas se emplea también en el desarrollo de medicamentos para establecer los perfiles farmacocinéticos de las sustancias objeto de estudio. O lo que es lo mismo: qué le pasa a un fármaco desde el momento en que entra en contacto con el organismo (por vía oral, parenteral…) hasta su eliminación del mismo. Hay que recordar que un fármaco es activo mientras sus concentraciones en sangre permanezcan dentro de una determinada ventana terapeutica. Concentraciones menores al límite inferior de la ventana implican inactividad y mayores, toxicidad.
De igual modo que se monitorizan las constantes vitales, se pueden monitorizar las concentraciones de los medicamentos en los pacientes. En la práctica clínica es un proceso habitual para estimar las dosis adecuadas de los medicamentos, sobre todo para compuestos con una estrecha ventana terapéutica o en casos en los que la respuesta del paciente no es la esperada. La monitorización de fármacos es un proceso indispensable en el desarrollo de medicamentos, antes de que puedan ser comercializados. También permite construir perfiles farmacocinéticos, es decir, medir las concentraciones en sangre de un determinado compuesto desde la aplicación hasta la eliminación, que permiten conocer parámetros indispensables (Imagen 4) para comprender su comportamiento. Para ello se emplea mayoritariamente la espectrometría de masas por la selectividad y sensibilidad que aporta. Además permite el desarrollo de métodos rápidos y robustos de análisis. Este conocimiento es esencial para poder utilizar los medicamentos o cualquier otro tipo de sustancias de forma segura.
Punto tres: buscar una aguja en un pajar
No sólo es importante saber qué buscar, sino que en muchos casos es necesario determinar mínimas cantidades de los compuestos a analizar, sobre todo en el caso de compuestos de elevada potencia. Un resultado positivo o negativo, por ejemplo en casos de consumo de drogas al volante, va a determinar el tipo y la cuantía del castigo. Lo mismo pasa en el deporte. La aparición de sustancias prohibidas es indicativo de dopaje, con sus múltiples consecuencias. Por todo ello, la cuantificación de sustancias tiene que ser lo más fiable posible y poder medir concentraciones, que en algunos casos, rondan los límites que permite la tecnología. Y la espectrometría de masas es una técnica de análisis selectiva y que permite determinar concentraciones del orden de las partes por billón, dependiendo de los compuestos a analizar y la matriz en la que se encuentran. Para que nos hagamos una idea, sería como encontrar un determinado grano en un metro cúbico de arena.
En definitiva, se puede afirmar que los espectrómetros de masas son los ojos del investigador para poder ver todos esos compuestos perdidos, los que aún no conocemos y los que sí, para obtener información que nos ayude a entender mejor diferentes procesos y a dar respuesta a múltiples preguntas, permitiendo el avance del conocimiento científico.
Sobre la autora: Nerea Ferreirós Bouzas se doctoró en la Facultad de Ciencia y Tecnología de la UPV/EHU y es investigadora en el Instituto de Farmacología Clínica de la Goethe-Universität de Fráncfort del Meno, Alemania.

