Periodo de semidesintegración

Cuando hablamos de la impureza de las muestras radiactivas pusimos como ejemplo que, de 1,000,000 de átomos de 218Po presentes en una muestra recién preparada, solo quedarían alrededor de 10,000 después de 20 min, y el resto se habría desintegrado en átomos de 214Pb y sus productos hijos. Solo 3 minutos después de la preparación de la muestra pura de 218Po el 50% de los átomos originalmente presentes en la muestra se habrían desintegrado. En el caso del radio (226Ra), la mitad de los átomos de radio en una muestra recién preparada de radio tardaría 1620 años en transformarse en átomos de radón.
Estos dos ejemplos ilustran el hecho experimental de que las muestras de elementos radiactivos presentan una gran diferencia en sus velocidades de desintegración. Estas diferentes velocidades son el resultado promedio de muchos eventos individuales de desintegración diferentes que ocurren al azar en una muestra. Si nos centramos en un átomo concreto de cualquier elemento radiactivo, nunca podemos saber cuándo se desintegrará; algunos pueden desintegrarse tan pronto como se producen, mientras que otros puede que nunca se desintegren. Aún así, se ha encontrado experimentalmente que dada una muestra que contenga átomos radiactivos de un mismo tipo [1], la fracción de estos átomos que se desintegra por segundo es inmutable [2] y siempre la misma para un número lo suficientemente grande de átomos de ese tipo. [3] Esta fracción es casi completamente independiente de todas las condiciones físicas y químicas, como temperatura, presión o combinación química. [4]
Este hecho experimental tiene consecuencias muy importantes. Digamos, por ejemplo, que 1 de cada 1000 de los átomos de una muestra pura recién preparada se desintegra durante el primer segundo. Entonces, cabe esperar que 1 de cada 1000 de los átomos restantes se desintegre durante el siguiente segundo. Igualmente, 1/1000 de los átomos que quedasen después de 10 s se desintegrarán durante el undécimo segundo, y así sucesivamente. De hecho, durante cualquier segundo siguiente, 1/1000 de los átomos que quedan al comienzo de ese segundo se desintegrarán, al menos hasta que el número de átomos restantes no sea lo suficientemente grande y que las predicciones se vuelvan muy inciertas.
Dado que la fracción de átomos que se desintegra por unidad de tiempo es una constante para cada tipo de átomo, el número de átomos que se desintegran por unidad de tiempo disminuirá en proporción al número decreciente de átomos que aún no han cambiado. En consecuencia, si hacemos una gráfica del porcentaje de átomos inalterados supervivientes en función del tiempo, se obtiene una curva como la de la figura siguiente.
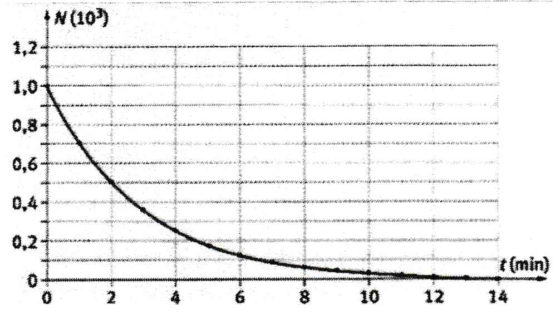
El número de átomos en una muestra que se desintegra por unidad de tiempo se denomina actividad de la muestra. Por lo tanto, la gráfica también representa la forma en que la actividad medida de una muestra disminuiría con el tiempo. La curva que muestra el número de átomos que no se han desintegrado aun en función del tiempo se aproxima asintóticamente al eje del tiempo; es decir, el número de átomos supervivientes se reduce, pero solo se acerca a cero [5]. Esta es otra forma de decir que no se puede asignar un “tiempo de vida” definido en la que todos los átomos originales de una muestra se habrán desintegrado.
Sin embargo, es posible especificar el tiempo requerido para que se desintegre cualquier fracción arbitraria de una muestra, la mitad, un tercio o el 67%, por ejemplo. Por conveniencia a la hora de hacer comparaciones, se optó en su momento por la fracción 1/2. Rutherford denominó half-life, periodo de semidesintegración [6], al tiempo necesario para la desintegración de la mitad de los átomos originales de una muestra pura (símbolo T1/2). Cada tipo de átomo radiactivo tiene un periodo de semidesintegración único [7].
Notas:
[1] Para muestras de un mismo isótopo. Introducimos el concepto de isótopo más adelante en la serie, por lo que ahora preferimos la perífrasis.
[2] En el sentido de que no puede alterarse.
[3] Esta frase en negrita es fundamental para comprender la radiactividad.
[4] Este hecho convierte a algunas especies radiactivas en excelentes relojes para distintos usos. Probablemente la técnica más conocida que hace uso de uno de estos relojes es la datación por carbono-14.
[5] Lo de que es una curva asintótica es una simplificación. Conforme la muestra se hace más pequeña nos encontraremos fluctuaciones estadísticas que serán significativas, por lo que la curva ya no será tal, sino una serie de escalones.
[6] Hay que apresurarse a decir que half-life no es vida media, sino semivida. Vida media es un concepto de física de partículas y se refiere a una partícula concreta. En radiactividad hablamos de una población de átomos, por tanto de semivida y, más concretamente de periodo de semidesintegración.
[7] Lo que implica que el periodo de semidesintegración de un elemento se puede utilizar para identificar el tipo de elemento radiactivo.
Sobre el autor: César Tomé López es divulgador científico y editor de Mapping Ignorance
Datación radiométrica — Cuaderno de Cultura Científica
[…] los árboles vivos de esa especie, los científicos pueden determinar su edad aproximada usando su periodo de semidesintegración. Por ejemplo, si solo queda la mitad de la cantidad original de carbono 14, entonces el árbol […]