El control nervioso de la respiración
La mayor parte de los animales necesitan respirar continuamente. Por esa razón, los movimientos que proporcionan o permiten el flujo de medio respiratorio al órgano correspondiente son generados por programas rítmicos innatos que corren a cargo de estructuras neuronales específicas y pueden operar independientemente de los centros encefálicos superiores. Esos centros procesan señales procedentes de quimiorreceptores que reciben información relativa a la concentración de los gases respiratorios en el fluido interno que los transporta. Y como consecuencia de la valoración de esa información emiten señales que regulan la concentración de esos gases mediante un sistema de retroalimentación negativa. La ventilación traqueal de insectos terrestres parece estar regulada mediante señales enviadas por los ganglios metatorácicos. Y en los vertebrados el ritmo respiratorio viene marcado por el centro respiratorio ubicado en el tronco encefálico.
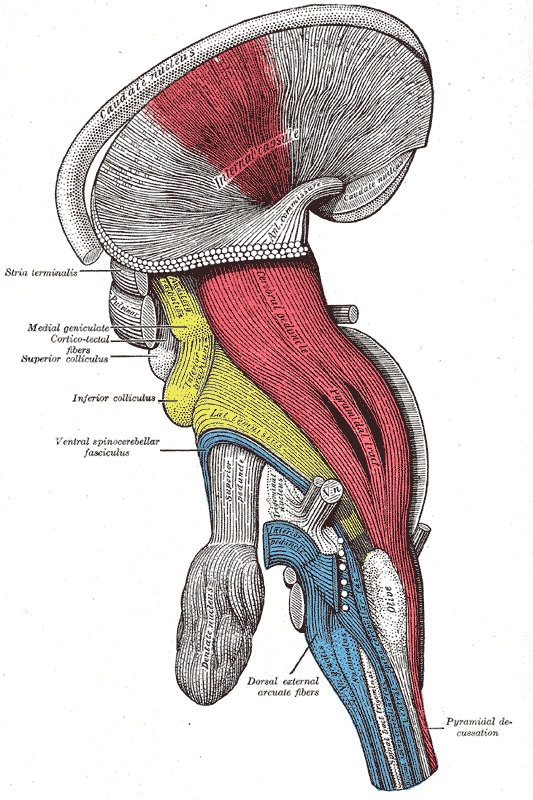
En los vertebrados, el control nervioso de la respiración tiene tres componentes: (1) el programa generador de patrones, para el ritmo alternante de inspiración/espiración; (2) los factores que regulan la intensidad de la ventilación (frecuencia y profundidad de la respiración) para ajustarla a las necesidades; y (3) los factores que modifican la actividad respiratoria para que sirva a otros propósitos (como hablar, por ejemplo); en este último caso, los centros superiores pueden tomar parte en el control.
En mamíferos, con independencia de cuál sea el nivel de consumo de oxígeno o de la producción de dióxido de carbono por parte de los tejidos, las tensiones parciales de oxígeno (tO2) y de dióxido de carbono (tCO2) de la sangre arterial que abandona los pulmones presentan una considerable constancia, lo que indica que ambas magnitudes están sometidas a un estricto control.
En los mamíferos, el principal centro de control respiratorio es el centro respiratorio medular, que consta de dos grupos o agregaciones de cuerpos celulares neuronales en el interior de la médula: el grupo respiratorio dorsal y el grupo respiratorio ventral. Pero además de ese centro principal, hay otro grupo respiratorio en el puente troncoencefálico (puente de Varolio), formado a su vez por dos áreas: el centro neumotáxico y el centro apnéustico.
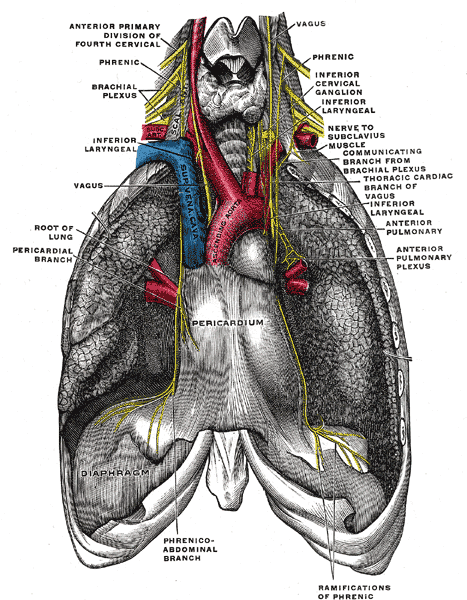
El nervio frénico y los nervios intercostales son los que transmiten las órdenes motoras al diafragma y músculos intercostales que provocan los movimientos rítmicos de contracción y relajación de la caja torácica. Los cuerpos celulares de esos nervios se encuentran en la médula espinal (espina dorsal) y reciben señales del centro respiratorio medular. Cuando esas neuronas motoras estimulan los músculos inspiratorios, provocan el movimiento de inspiración; la espiración se produce cuando esas neuronas no transmiten impulsos. El grupo dorsal del centro respiratorio medular consta principalmente de neuronas inspiratorias, cuyas fibras descendentes establecen sinapsis con las motoneuronas de la médula espinal citadas. El grupo ventral se encuentra interconectado con el dorsal, y está compuesto tanto por fibras inspiratorias como espiratorias. Pero este grupo se encuentra inactivo durante la respiración normal; solo interviene cuando debe elevarse la ventilación y es especialmente importante para intensificar la espiración. Durante la respiración normal (tranquila) no se envían señales a través de las vías descendentes de las neuronas espiratorias. Las motoneuronas que inervan los músculos espiratorios (abdominal e intercostales internos) solo son estimuladas cuando se requiere una espiración activa. Además, las neuronas inspiratorias del grupo ventral, cuando son estimuladas por el grupo dorsal, aceleran la actividad inspiratoria cuando las demandas ventilatorias aumentan.
La generación del ritmo respiratorio parece descansar en un área denominada médula rostral ventromedial, que se encuentra en la zona superior del grupo respiratorio ventral, en la que se han localizado redes neuronales que generan una actividad marcapasos. No obstante, no se conoce muy bien el mecanismo que da lugar a los movimientos respiratorios rítmicos.
Por su parte, los centros neumotáxico y apnéustico del puente de Varolio ejercen un control fino sobre el centro respiratorio medular que ayuda a suavizar los movimientos respiratorios. El centro neumotáxico envía señales al grupo respiratorio dorsal que ayudan a desconectar las neuronas inspiratorias, limitando así la duración de las inspiraciones. Por el contrario, el centro apneústico impide la desconexión de esas mismas neuronas, las inspiratorias. En ese sistema de contrapesos domina el centro neumotáxico, lo que contribuye a poner límites a la inspiración, permitiendo que la espiración curse con normalidad. Sin la acción del centro apnéustico el ciclo respiratorio consistiría en prolongadas espiraciones interrumpidas por inspiraciones rápidas y muy bruscas.
Como es lógico, la tasa ventilatoria se ajusta para satisfacer las demandas metabólicas de cada momento. Y en ese ajuste se valoran tres indicadores diferentes, la tO2, la tCO2 y el pH, aunque como veremos al final, hay circunstancias en que intervienen otras señales.
En mamíferos, la tO2 arterial es monitorizada mediante unos quimiorreceptores conocidos como cuerpos carótidos y cuerpos aórticos, que se localizan en las bifurcaciones de las arterias carótidas y en el arco de la aorta, respectivamente. En los peces hay quimiorreceptores similares a los de mamíferos pero se localizan en las branquias de forma difusa, y cuando esos receptores detectan una reducción en la tO2 se produce un aumento de la ventilación branquial. Sin embargo, en los vertebrados que respiran en aire las cosas son diferentes. Tiene que caer la tO2 hasta valores tan bajos como 60 mmHg (¡un 40%!) para que se produzca una respuesta por parte de los sistemas de control. La razón de que no haya respuesta a valores superiores de tO2 es que aunque estos sean relativamente bajos, el porcentaje de saturación de la hemoglobina es todavía alto (alrededor del 90% se encuentra combinada con O2). Sin embargo, por debajo de 60 mmHg la saturación del pigmento se reduce muy rápidamente, por lo que la situación se puede volver muy peligrosa y conducir a la asfixia. El pigmento amortigua los efectos de variaciones no demasiado grandes en la tO2 arterial, por lo que funciona, de hecho, como un reservorio de oxígeno que asegura el suministro a los tejidos siempre que la tensión arterial de oxígeno no se reduzca en exceso.
Un aspecto ciertamente llamativo de este sistema receptor es que al responder a la tO2, cualquier factor que reduzca la fracción de O2 combinado con el pigmento pero que no provoque una bajada en aquella, puede resultar fatal, ya que puede darse la circunstancia de que se produzca una caída muy fuerte en el contenido total de O2 en la sangre y ello no dé lugar a una respuesta respiratoria. Es lo que ocurre, por ejemplo, cuando altas cantidades de monóxido de carbono (CO) se unen con la hemoglobina desplazando al O2 de sus sitios de unión. Quienes se intoxican con CO no experimentan una elevación de la tasa ventilatoria en respuesta a la intoxicación porque el CO no provoca una reducción en la tO2 pero sí en el contenido total de oxígeno en la sangre.
Bajo condiciones de reposo, la tCO2 es el parámetro que más importancia tiene en el ajuste de la tasa ventilatoria en mamíferos. Al contrario de lo que ocurre con la tO2, pequeños cambios en la tCO2 dan lugar a una respuesta en la ventilación pulmonar. Un exceso de CO2 en la sangre genera una respuesta refleja a cargo de los centros respiratorios que provocan un aumento en la ventilación y, como consecuencia, la eliminación de tal exceso y la restauración de su nivel normal. Lo contrario ocurre cuando la tCO2 se reduce por debajo del nivel de referencia. La mayoría de los peces también ajustan su tasa ventilatoria en respuesta a las variaciones sanguíneas en la tCO2; se cree que los centros respiratorios reciben las señales de quimiorreceptores branquiales.
En la mayor parte de los animales que respiran en aire no se monitoriza la tCO2 arterial; de hecho, los cuerpos carótidos y aórticos responden muy levemente a los cambios en el nivel arterial de CO2. De mucha mayor importancia son los quimiorreceptores centrales, que se encuentran en la médula, en una posición muy próxima al centro respiratorio. Aunque en realidad, esos quimiorreceptores no monitorizan la concentración de CO2 directamente, sino la de protones –que depende de la anterior- en el líquido extracelular del encéfalo. Los peces sin embargo, parecen carecer de receptores centrales de ese tipo. De hecho, lo más probable es que los receptores centrales aparecieran en los sarcopterigios (peces pulmonados).
Se da la circunstancia de que el CO2 atraviesa la barrera hematoencefálica con gran facilidad, al contrario de lo que ocurre con los H+. Por ello, cuando se produce una elevación de la concentración de estos últimos en el líquido extracelular encefálico ello es señal de que se ha producido un aumento en la concentración de CO2 en el encéfalo.
El gran efecto que ejercen los quimiorreceptores centrales sobre el centro respiratorio es el responsable de que no podamos dejar de respirar a voluntad durante más de un minuto (las personas normales, claro). Cuando dejamos de respirar, la concentración de CO2 no deja de aumentar, porque el metabolismo no cesa y, en paralelo, también aumenta la concentración de protones. Ese aumento acaba ejerciendo un efecto tal sobre el centro respiratorio, que este supera las órdenes provenientes de los centros superiores y provoca la ejecución de los movimientos de los correspondientes músculos.
Dependiendo de las demandas de oxígeno del organismo y de la correspondiente necesidad de eliminar dióxido de carbono, la ventilación alveolar puede llegar a multiplicarse hasta por veinte. Lo curioso es que esa elevación no parece ser provocada por los cambios en las concentraciones de O2, CO2 y H+. De hecho, la concentración arterial de ninguna de esas sustancias experimenta cambios significativos al elevarse la tasa de ventilación pulmonar. Y por otro lado, el aumento de esa tasa se produce en el mismo instante en que se intensifica la actividad que da lugar a la elevación de las demandas metabólicas, pero mucho antes de que haya dado tiempo a que varíen las concentraciones de los gases respiratorios y de los protones en una medida suficiente como para provocar una respuesta regulatoria. Para eso habría hecho falta que transcurriera al menos un minuto, pero la respiración se acelera enseguida.
Son otros los mecanismos que determinan la aceleración de los movimientos respiratorios al iniciarse una actividad física. Y se han sugerido los siguientes: (1) Reflejos cuya génesis se encontraría en los propios movimientos musculares cuya actividad ha de sostenerse y que vendrían activados por señales procedentes de músculos y articulaciones; (2) elevación de la temperatura corporal; (3) liberación de adrenalina; y (4) control anticipatorio a cargo de la corteza cerebral. Como se ha señalado, se trata de posibles mecanismos; todos son verosímiles, pero ninguno de ellos o combinación de varios resultan satisfactorios para explicar el efecto tan marcado e intenso que ejerce el inicio de la actividad sobre la tasa ventilatoria.
Fuentes:
David Randall, Warren Burggren & Kathleen French (2002): Eckert Animal Physiology: Mechanisms and Adaptations 5th ed.; Freeman & Co, New York
Lauralee Sherwood, Hillar Klandorf & Paul H. Yancey (2005): Animal Physiology: from genes to organisms. Brooks/Cole, Belmont.
Sobre el autor: Juan Ignacio Pérez (@Uhandrea) es catedrático de Fisiología y coordinador de la Cátedra de Cultura Científica de la UPV/EHU

Hitos en la red #204 | Enlace Recomendado | Naukas
[…] de alguien que diga que deja de respirar a voluntad? Ya. Pues va a ser que no: El control nervioso de la respiración por Juan Ignacio Pérez […]
Regulación de la circulación (1): control del sistema cardiovascular – Cuaderno de Cultura Científica
[…] recibe inputs de otras regiones encefálicas, como el centro respiratorio (del que hablamos aquí), el hipotálamo, la amígdala (al que nos referimos aquí) y la corteza […]
Respuesta de los sistemas respiratorio y cardiovascular al ejercicio físico – Cuaderno de Cultura Científica
[…] para dar respuesta a las demandas metabólicas elevadas que impone la actividad física. Ya vimos aquí como se regula la respiración, y aquí y aquí, la circulación sanguínea, que son las dos […]
Efectos de la respiración sobre el cerebro | Sección de Medicina, Salud y Bienestar
[…] Se trata de unas 350 neuronas distribuidas por el sistema nervioso central. Lo que las hace diferentes del resto es que se activan más cuanto más rápida sea la respiración. Esto es importante porque estas neuronas mandan estímulos a otras partes del cerebro. […]
Maximiliano P. González
Leído este capítulo de la Fisiología animal, ya de antemano, por un episodio casual de alguien que me anunció el fallecimiento de su marido, intuí que la vía progresiva del Covid-19, una vez penetrado en la mucosa bucofaríngea y nasal, podía ser la de los pares nerviosos del cerebro (Fila Olfatoria, par I y la del Glosofaríngeo, par IX) por los síntomas primarios de la anosmia y la disfunción gustativa: El virus seguiría por los axones mielínicos de estos nervios hasta llegar a las proximidades del Centro Respiratorio de la Formatio Reticularis en la médula oblongata del tronco cerebral, al cual invadiría el virus paralizando el sistema de fuelle del aparato respiratorio. Una vez paralizados los músculos de la respiración, el organismo se halla sin aporte de oxígeno e hipersaturado de anhídrido carbónico. Como resultado de ello, el cuadro metabólico del organismo entra en caos, por la falta de energía que se genera en el Ciclo de Krebs – cadena respiratoria – y absoluto descontrol del círculo del del ácido cítrico, del cual derivan muchas reacciones bioquímicas, entre ellas el metabolismo de las grasas y la regeneración de la hemoglobina en el paso del alfa-ketoglutarat con la participación de la SH- coenz.A, se oxida y tras desprendimiento de CO2, se forma el ácido sucínico que con la sumación del glicocol, se anaboliza el ácido delta-aminolevulínico hacia el porfobilinógeno hacia el Hem de la hemoglobina. Si esto no puede realizarse significa que la sangre no puede transportar el oxígeno, que ya de por sí no existe. El sistema nervioso, muy sensible a la anoxia, así como otros tejidos, por lo que aparecen numerosas enfermedades que dejarán secuelas según la ausencia de este oxígeno. Si a esta gravísima situación se le añade el exceso de CO2 acumulado por la ausencia de espiración la catástrofe está servida.