Visible y ultravioleta

Visible. Longitudes de onda de 7·10-7 m a 4·10-7 m; frecuencias entre 4·1014 y 8·1014 Hz
Esta pequeña banda de frecuencias se conoce como luz visible porque los receptores visuales de los ojos humanos solo son sensible a estas frecuencias. Si la luz de este rango de frecuencias atraviesan un prisma de cristal o gotas de lluvia, la refracción diferente que experimentan las distintas frecuencias hace que los humanos perciban cada una como un color diferente (esta descomposición la llaman arco iris). Los humanos discriminan entre el rojo en un extremo (4·1014Hz) y el violeta en el otro (8·1014 Hz ).
Las frecuencias de la luz visible son aquellas en las que el Sol irradia energía en grandes cantidades. A lo largo de la evolución el ojo humano se ha ido especializando en usar esta abundancia. En la lucha por la supervivencia y la reproducción los humanos se convirtieron en criaturas diurnas. Otras especies, como muchos depredadores nocturnos, lo que incluye a gatos, perros y algunos marsupiales, han desarrollado la capacidad de usar pequeñas cantidades de luz visible para la visión nocturna, y algunos son incluso capaces de ver usando frecuencias que caen en la región infrarroja, invisible para los humanos.
Ultravioleta. Longitudes de onda de 10-7 m a 10-8 m; frecuencias entre 1015 y 1016 Hz
Las ondas electromagnéticas con frecuencias, y energías, por encima del rango visible, a saber, ultravioleta, rayos X y rayos gamma, tienen en común que pueden dañar el tejido vivo, y pueden causar cáncer y mutaciones genéticas.
Si bien los rayos X y los gamma son radiaciones perfectamente naturales en nuestro entorno, son mucho menos abundantes que los rayos ultravioletas, que nos llegan directamente del Sol y que, en cantidades moderadas, necesitamos para vivir. La existencia de una capa en la atmósfera disminuye de forma importante la cantidad de radiación ultravioleta que llega a la superficie terrestre. Esta capa contiene un alótropo del oxígeno, el ozono (O3), que la da nombre.
En condiciones de la superficie terrestre dos átomos de oxígeno se combinan para formar oxígeno molecular, O2, que es el que respiramos. Sin embargo, en determinadas circunstancias, como las que provoca un rayo, tres átomos de oxígeno se unen débilmente para formar ozono. Este ozono en días calurosos puede combinarse con los gases de escape de los motores de combustión, creando las nubes de contaminación de las grandes ciudades. Sin embargo, en la parte alta de la atmósfera, el hecho de que esta molécula vibre con la frecuencia de los rayos ultravioletas hace que absorba (excitándose) y refleje parte de esta radiación de vuelta al espacio (al relajarse la molécula, emite en todas direcciones, incluidas la del espacio).
Desafortunadamente el desarrollo de los cloroflurocarbonos en los años treinta del siglo XX, ampliamente usados en la industria y en los hogares del mundo desarrollado en aerosoles y sistemas de refrigeración. Estas sustancias, tal y como se descubrió cincuenta años más tarde, cuando se emiten a la atmósfera alcanzan las capas superiores donde reaccionan con el ozono convirtiéndolo en oxígeno molecular, en una reacción en en la que el cloro actúa como catalizador y donde la energía la proporciona la ultravioleta. Un solo ion cloro es capaz de destruir miles de moléculas de ozono.
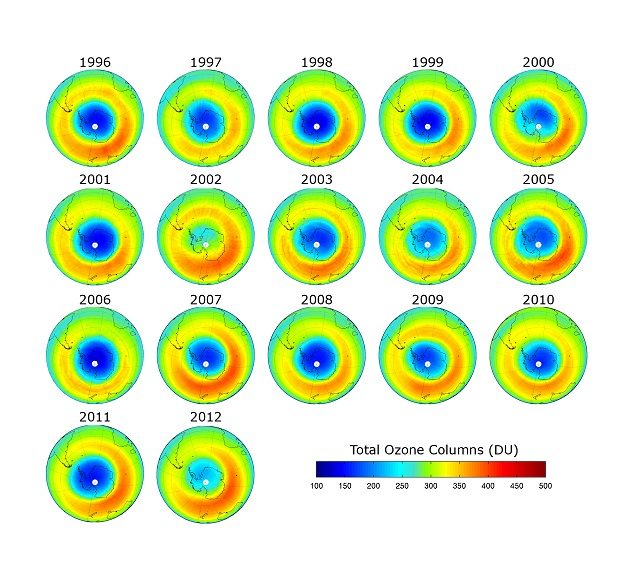
La desaparición de la capa de ozono, especialmente apreciable en los polos terrestres, originó un aumento de los cánceres de piel y de las cataratas oculares. Los cloroflurocarbonos se prohibieron en el año 2000, pero el cloro en la atmósfera emitido durante setenta años aún continuará ralentizando la restauración de la capa de ozono bastantes años más.
Sobre el autor: César Tomé López es divulgador científico y editor de Mapping Ignorance

Máquinas, Equipamientos, Aparatos
[…] en https://culturacientifica.com/2016/09/13/visible-y-ultravioleta/ […]