Un modelo simple de gas

¿Cuáles son las diferencias entre un gas y un líquido o un sólido? Sabemos por experiencia que, si no se comprimen, los líquidos y los sólidos tienen volumen definido. Incluso si sus formas cambian, todavía ocupan la misma cantidad de espacio. Un gas, por otra parte, se expandirá espontáneamente para llenar cualquier recipiente (como una habitación). Si no está confinado, saldrá y se extenderá en todas direcciones [1].
Los gases tienen densidades bajas en comparación con los de líquidos y sólidos, típicamente alrededor de 1000 veces más pequeñas. Por lo tanto, las moléculas [2] de gas suelen estar relativamente alejadas unas de otras. En el modelo de un gas que vamos a construir, podemos suponer razonablemente que las fuerzas entre las moléculas actúan sólo a distancias muy cortas. En otras palabras, las moléculas de gas se consideran que se mueven libremente la mayor parte del tiempo. En los líquidos, las moléculas están más juntas, las fuerzas actúan continuamente entre ellas y les impiden que se separen demasiado. En los sólidos, las moléculas suelen estar aún más juntas, y las fuerzas entre ellas las mantienen en una disposición más (cristales) o menos (vidrios) definida.
Antes de continuar quizás convengan recordar que vamos a plantear un modelo teórico de un gas. Este modelo existirá, por tanto, solo en nuestra imaginación. Al igual que los puntos, las líneas, los triángulos y las esferas que se estudian en geometría, este modelo teórico podrá ser tratado matemáticamente. Los resultados de este tratamiento pretenden comprender el mundo real aunque, por supuesto, previamente el modelo tendrá que ser comprobado experimentalmente a fin de ver si se aproxima a la realidad.
Nuestro modelo inicial de un gas es por tanto muy simple, siguiendo el consejo de Newton de comenzar con las hipótesis más simples. Asumiremos que las moléculas son pequeñas esferas o grupos de esferas que no ejercen ninguna fuerza en las demás salvo cuando hacen contacto. Además, supondremos que todas las colisiones de estas esferas son perfectamente elásticas, esto es, la energía cinética total de dos esferas es la misma antes y después de chocar, no hay pérdidas.
Nuestro modelo teórico considera que el gas consiste en un gran número de partículas muy pequeñas en movimiento rápido y desordenado. «Un gran número» significa algo así como un trillón (1018) o más partículas en una muestra tan pequeña como una burbuja en un refresco. «Muy pequeño» significa un diámetro claramente inferior a un nanómetro (10-9 m) para cada una de esas partículas. «Movimiento rápido» significa una velocidad media a temperaturas normales de unos cuantos cientos de metros por segundo.
El concepto “desordenado” es algo más prolijo de explicar. Los teóricos cinéticos del siglo XIX supusieron que cada molécula individual se movía de manera definida, determinada por las leyes del movimiento de Newton. Por supuesto, en la práctica es imposible seguir billones y billones de partículas al mismo tiempo. Se mueven en todas direcciones y cada partícula cambia su dirección y velocidad durante las colisiones con otras partículas o con la pared del recipiente. Por lo tanto, no podemos hacer una predicción definida del movimiento de ninguna partícula individual. Por contra, debemos contentarnos con describir el comportamiento promedio de grandes colecciones de partículas. De un momento a otro, cada molécula individual se comporta de acuerdo con las leyes del movimiento. Pero es más fácil describir el comportamiento promedio, y asumir completa ignorancia sobre cualquier movimiento individual.
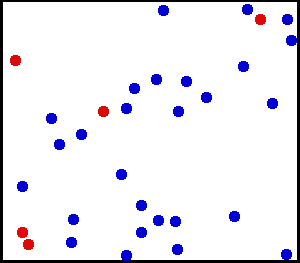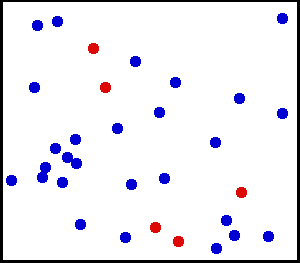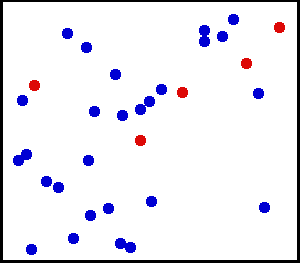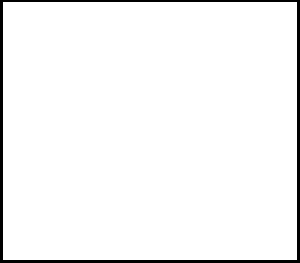
Para ver por qué esto es así, imagina los resultados de lanzar al aire un gran número de monedas a la vez. Si asumimos que las monedas se comportan al azar, puedes predecir con confianza que lanzar un millón de monedas dará aproximadamente 50% de caras y 50% de cruces. El mismo principio se aplica a las moléculas de gas rebotando en un contenedor. Puedes asumir con seguridad, por ejemplo, que se mueven en una dirección tantas como lo hacen en cualquier otra. Además, en un momento dado el mismo número de moléculas es igualmente probable que se encuentre en cualquier centímetro cúbico de espacio dentro del contenedor como en cualquier otro. «Desordenado», entonces, significa que las velocidades y las posiciones se distribuyen al azar. Cada molécula es tan probable que esté moviéndose a la derecha como a la izquierda (o en cualquier otra dirección). Es tan probable que esté cerca del centro como cerca del borde (o en cualquier otra posición).
Ya tenemos construido nuestro modelo. Ahora a ver cómo se comporta y a ver que extraemos de ello. Eso será en las próximas entregas de esta serie.
Notas:
[1] El confinamiento no implica la existencia de un contenedor, aunque en este texto asumamos implícitamente que sí por simplicidad. Un gas puede estar confinado por la gravedad, como en una estrella o, sin ir más lejos, en la atmósfera, aunque no sea un confinamiento completamente estanco.
[2] Empleamos “moléculas” y no “átomos” por generalidad del concepto. Los gases constituidos por átomos que no forman parte de una molécula son una minoría frente a todos los gases moleculares posibles.
Sobre el autor: César Tomé López es divulgador científico y editor de Mapping Ignorance

Hitos en la red #180 – Naukas
[…] Un modelo simple de gas […]
Los antecedentes de la teoría cinética – Cuaderno de Cultura Científica
[…] las moléculas. Para ello hemos elegido el sistema más simple, un gas, para el que hemos descrito un modelo también muy simple y nos disponemos a ver qué podemos deducir de la hipótesis de que los moléculas no solo existen, […]
La distribución de velocidades moleculares de Maxwell – Cuaderno de Cultura Científica
[…] con nuestro modelo simple y las ideas de Clausius, hay que empezar por el principio, esto es, por las volocidades que […]
La teoría cinética y la segunda ley de la termodinámica – Cuaderno de Cultura Científica
[…] modelo de la teoría cinética puede explicar el comportamiento de un gas cuando es comprimido o expandido, calentado o enfriado. […]